− выбраны вещества, и записано молекулярное уравнение реакции ионного обмена;
Гидросульфит натрия (sodium hydrogen sulphite, sodium bisulphite) — антиоксидант и консервант (E222). Химическая формула — NaHSO3.
- Главная
- Продукция
- Реактивы
- Бисульфат натрия
Поиск
Каталог
Гидросульфат натрия (кислый сернокислый натрий, бисульфат натрия) — кислая соль натрия и серной кислоты с формулой NaHSO4, бесцветные кристаллы. Образует кристаллогидрат NaHSO4·H2O. Гидросульфат натрия представляет собой белое сухое кристаллическое вещество плотностью 2,476 кг/куб.дм; безводный продукт сильно гигроскопичен.
Получение гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
Распространены 2 промышленных метода. В обоих один из реагентов — серная кислота, а второй — гидроксид или хлорид натрия. Полученный водный раствор целевого продукта затем формируют в гранулы; целесообразно купить гидросульфат натрия именно в гранулированном виде, гораздо более удобном для применения и хранения.
- Гидросульфат натрия получают действием избытка концентрированной серной кислоты на едкий натр:
гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- Гидросульфат натрия образует бесцветные кристаллы триклинной сингонии, пространственная группа P , параметры ячейки = 0,7005 нм, = 0,7125 нм, = 0,6720 нм, = 95,93°, = 92,31°, = 75,52°, . При нагревании претерпевает два полиморфных перехода при 140 и 170 °C.
- Кристаллогидрат гидросульфата натрия — бесцветные гигроскопические кристаллы моноклинной сингонии, пространственная группа A a, параметры ячейки = 0,8213 нм, = 0,7812 нм, = 0,7805 нм, = 120,04°, .
гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- При нагревании гидросульфат натрия переходит в пиросульфат натрия:
- При подщелачивании гидросульфат натрия переходит в сульфат:
- При спекании гидросульфат натрия взаимодействует с солями:
гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- Как флюс в цветной металлургии.
- Как реагент для перевода труднорастворимых окислов в растворимые сульфаты.
- Зарегистрирован в качестве пищевой добавки E514.
- в виде порошка или гранул в качестве реагента, понижающего уровень рН в бассейнах
Легкая и пищевая промышленность, металлообработка, коммунальное хозяйство, прикладные отрасли. Используется прежде всего как подкисляющий реагент с доступной ценой.
В промышленности гидросульфат натрия применяется в составе растворов для отделки кожи и текстильных материалов, а также при финишной обработке металлов: гальванизации, лакировании и др. Значительны объемы его использования в виде компонента бытовых чистящих средств. Также этот реагент применяется для подкисления воды в процессе хлорирования, например, при обеззараживании бассейнов.
Гидросульфат натрия одобрен как пищевая добавка в корма домашних животных; в этом направлении его назначение заключается в снижении щелочности мочи, что способствует предупреждению мочекаменной болезни у кошек. Гидросульфат натрия признан также безопасной пищевой добавкой в продовольственные продукты для человека обозначение E514ii по номенклатуре Евросоюза). Обладает уникальной особенностью — снижает pH среды без придания кислого вкуса; в таком качестве гидросульфат натрия используется в производстве множества продуктов питания: напитков, соусов и т.д. Актуально его применение в колбасных изделиях — гидросульфат натрия ингибирует нежелательное изменение цвета готового продукта при контакте с атмосферным кислородом.
В ювелирной отрасли гидросульфат натрия служит основой травильных растворов, удаляющих слой окислов с поверхностей, подвергнутых нагреванию в ходе ювелирной обработки.
- Главная
- Продукция
- Реактивы
- Гидросульфат натрия
Поиск
Каталог
Гидросульфат натрия (кислый сернокислый натрий, бисульфат натрия) — кислая соль натрия и серной кислоты с формулой NaHSO4, бесцветные кристаллы. Образует кристаллогидрат NaHSO4·H2O. Гидросульфат натрия представляет собой белое сухое кристаллическое вещество плотностью 2,476 кг/куб.дм; безводный продукт сильно гигроскопичен.
Получение гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
Распространены 2 промышленных метода. В обоих один из реагентов — серная кислота, а второй — гидроксид или хлорид натрия. Полученный водный раствор целевого продукта затем формируют в гранулы; целесообразно купить гидросульфат натрия именно в гранулированном виде, гораздо более удобном для применения и хранения.
- Гидросульфат натрия получают действием избытка концентрированной серной кислоты на едкий натр:
гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- Гидросульфат натрия образует бесцветные кристаллы триклинной сингонии, пространственная группа P , параметры ячейки = 0,7005 нм, = 0,7125 нм, = 0,6720 нм, = 95,93°, = 92,31°, = 75,52°, . При нагревании претерпевает два полиморфных перехода при 140 и 170 °C.
- Кристаллогидрат гидросульфата натрия — бесцветные гигроскопические кристаллы моноклинной сингонии, пространственная группа A a, параметры ячейки = 0,8213 нм, = 0,7812 нм, = 0,7805 нм, = 120,04°, .
гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- При нагревании гидросульфат натрия переходит в пиросульфат натрия:
- При подщелачивании гидросульфат натрия переходит в сульфат:
- При спекании гидросульфат натрия взаимодействует с солями:
гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- Как флюс в цветной металлургии.
- Как реагент для перевода труднорастворимых окислов в растворимые сульфаты.
- Зарегистрирован в качестве пищевой добавки E514.
- в виде порошка или гранул в качестве реагента, понижающего уровень рН в бассейнах
Легкая и пищевая промышленность, металлообработка, коммунальное хозяйство, прикладные отрасли. Используется прежде всего как подкисляющий реагент с доступной ценой.
В промышленности гидросульфат натрия применяется в составе растворов для отделки кожи и текстильных материалов, а также при финишной обработке металлов: гальванизации, лакировании и др. Значительны объемы его использования в виде компонента бытовых чистящих средств. Также этот реагент применяется для подкисления воды в процессе хлорирования, например, при обеззараживании бассейнов.
Гидросульфат натрия одобрен как пищевая добавка в корма домашних животных; в этом направлении его назначение заключается в снижении щелочности мочи, что способствует предупреждению мочекаменной болезни у кошек. Гидросульфат натрия признан также безопасной пищевой добавкой в продовольственные продукты для человека обозначение E514ii по номенклатуре Евросоюза). Обладает уникальной особенностью — снижает pH среды без придания кислого вкуса; в таком качестве гидросульфат натрия используется в производстве множества продуктов питания: напитков, соусов и т.д. Актуально его применение в колбасных изделиях — гидросульфат натрия ингибирует нежелательное изменение цвета готового продукта при контакте с атмосферным кислородом.
В ювелирной отрасли гидросульфат натрия служит основой травильных растворов, удаляющих слой окислов с поверхностей, подвергнутых нагреванию в ходе ювелирной обработки.
- Главная
- Продукция
- Реактивы
- Кислый сернокислый натрий
Поиск
Каталог
Кислый сернокислый натрий
Гидросульфат натрия (кислый сернокислый натрий, бисульфат натрия) — кислая соль натрия и серной кислоты с формулой NaHSO4, бесцветные кристаллы. Образует кристаллогидрат NaHSO4·H2O. Гидросульфат натрия представляет собой белое сухое кристаллическое вещество плотностью 2,476 кг/куб.дм; безводный продукт сильно гигроскопичен.
Получение гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
Распространены 2 промышленных метода. В обоих один из реагентов — серная кислота, а второй — гидроксид или хлорид натрия. Полученный водный раствор целевого продукта затем формируют в гранулы; целесообразно купить гидросульфат натрия именно в гранулированном виде, гораздо более удобном для применения и хранения.
- Гидросульфат натрия получают действием избытка концентрированной серной кислоты на едкий натр:
гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- Гидросульфат натрия образует бесцветные кристаллы триклинной сингонии, пространственная группа P , параметры ячейки = 0,7005 нм, = 0,7125 нм, = 0,6720 нм, = 95,93°, = 92,31°, = 75,52°, . При нагревании претерпевает два полиморфных перехода при 140 и 170 °C.
- Кристаллогидрат гидросульфата натрия — бесцветные гигроскопические кристаллы моноклинной сингонии, пространственная группа A a, параметры ячейки = 0,8213 нм, = 0,7812 нм, = 0,7805 нм, = 120,04°, .
гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- При нагревании гидросульфат натрия переходит в пиросульфат натрия:
- При подщелачивании гидросульфат натрия переходит в сульфат:
- При спекании гидросульфат натрия взаимодействует с солями:
гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- Как флюс в цветной металлургии.
- Как реагент для перевода труднорастворимых окислов в растворимые сульфаты.
- Зарегистрирован в качестве пищевой добавки E514.
- в виде порошка или гранул в качестве реагента, понижающего уровень рН в бассейнах
Легкая и пищевая промышленность, металлообработка, коммунальное хозяйство, прикладные отрасли. Используется прежде всего как подкисляющий реагент с доступной ценой.
В промышленности гидросульфат натрия применяется в составе растворов для отделки кожи и текстильных материалов, а также при финишной обработке металлов: гальванизации, лакировании и др. Значительны объемы его использования в виде компонента бытовых чистящих средств. Также этот реагент применяется для подкисления воды в процессе хлорирования, например, при обеззараживании бассейнов.
Гидросульфат натрия одобрен как пищевая добавка в корма домашних животных; в этом направлении его назначение заключается в снижении щелочности мочи, что способствует предупреждению мочекаменной болезни у кошек. Гидросульфат натрия признан также безопасной пищевой добавкой в продовольственные продукты для человека обозначение E514ii по номенклатуре Евросоюза). Обладает уникальной особенностью — снижает pH среды без придания кислого вкуса; в таком качестве гидросульфат натрия используется в производстве множества продуктов питания: напитков, соусов и т.д. Актуально его применение в колбасных изделиях — гидросульфат натрия ингибирует нежелательное изменение цвета готового продукта при контакте с атмосферным кислородом.
В ювелирной отрасли гидросульфат натрия служит основой травильных растворов, удаляющих слой окислов с поверхностей, подвергнутых нагреванию в ходе ювелирной обработки.
Задания 31. Диссоциация электролитов. Реакции ионного обмена.
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
перманганат калия, гидрокарбонат калия, сульфит натрия, сульфат бария, гидроксид калия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
K + + HCO3 — + K + + OH — = 2K + + CO3 2- + H2O
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
гидрокарбонат натрия, алюминат натрия, бромид калия, углекислый газ, концентрированная серная кислота.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
азот, хлороводород, оксид фосфора (V), диоксид марганца, ацетат калия.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
CH3COOK + HCl = CH3COOH + KCl
CH3COO — + K + + H + + Cl — = CH3COOH + K + + Cl —
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
серная кислота, оксид серы (VI), гидроксид натрия, бром, силикат натрия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Первый вариант ответа:
Второй вариант ответа:
2Na + + 2OH — + 2H + + SO4 2- = 2Na + + SO4 2- + H2O
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
углекислый газ, сульфат натрия, бром, бромоводород, сульфит калия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
2H + + 2Br — + 2K + + SO3 2- = 2K + + 2Br — + H2O + SO2
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
гидрокарбонат кальция, углерод, сульфид меди, азотная кислота, тетрагидроксоалюминат натрия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
пероксид водорода, фосфат лития, гидрокарбонат калия, гидроксид хрома (III), гидроксид калия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Первый вариант ответа:
K + + OH — + K + + HCO3 — = 2K + + CO3 2- + H2O
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
карбонат натрия, иодоводородная кислота, оксид серы (IV), гидроксид железа (III), хлорид алюминия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
2H + + 2I — + 2Na + + CO3 2- = 2Na + + 2I — + H2O + CO2
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
сульфид железа (II), гидроксид натрия, гидроксид алюминия, нитрит натрия, хлорид аммония. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Na + + OH — + NH4 + + Cl — = Na + + Cl — + NH3 + H2O
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
иодид натрия, ацетат бария, уксусная кислота, серная кислота, угарный газ. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Так как в левой и правой частях полного ионного уравнения не обнаруживаются одинаковые ионы, сокращенное ионное уравнение будет совпадать с полным ионным.
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
оксид железа (II), хлорид бария, гидроксид натрия, оксид кремния (IV), концентрированная азотная кислота. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
гидроксид натрия, дихромат калия, хлорид бария, диоксид кремния, соляная кислота. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
HCl + NaOH = NaCl + H2O
H + + Cl — + Na + + OH — = Na + + Cl — + H2O
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
дихромат калия, сульфат меди, серная кислота, бромид калия, гидроксид алюминия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
азотная кислота, гидроксид калия, бром, гидроксид хрома (III), серная кислота. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Первый вариант ответа:
Второй вариант ответа:
2K + + 2OH — + 2H + + SO4 2- = 2K + + SO4 2- + 2H2O
Третий вариант ответа:
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
карбонат бария, оксид меди (I), концентрированная серная кислота, гидрокарбонат натрия, дихромат натрия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Первый вариант ответа:
Так как в левой и правой частях полного ионного уравнения не обнаруживаются одинаковые ионы, сокращенное ионное уравнение будет совпадать с полным ионным.
Второй вариант ответа:
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
нитрат калия, углекислый газ, алюминий, гидрофосфат калия, гидроксид калия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
K + + OH — + 2K + + HPO4 2- = 3K + + PO4 3- + H2O
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
оксид фосфора (III), азотная кислота, оксид железа (III), оксид серы (IV), карбонат кальция. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
гидроксид алюминия, сульфат меди (II), нитрат железа (II), концентрированная азотная кислота, гидроксид калия
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Первый вариант ответа:
Второй вариант ответа:
Fe 2+ + 2NO3 — + 2K + + 2OH — = Fe(OH)2 + 2K + + 2NO3 —
Третий вариант ответа:
Cu 2+ + SO4 2- + 2K + + 2OH — = Cu(OH)2 + 2K + + SO4 2-
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
сульфат бария, сульфид калия, сульфат натрия, ацетат бария, перманганат калия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
2Na + + SO4 2- + 2CH3COO — + Ba 2+ = BaSO4 + 2CH3COO — + 2Na +
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
раствор серной кислоты, гидроксид меди (II), дихромат калия, диоксид кремния, сульфат железа (II). Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
ПрименениеПравить
- Как флюс в цветной металлургии.
- Как реагент для перевода труднорастворимых окислов в растворимые сульфаты.
- Зарегистрирован в качестве пищевой добавки E514.
- в виде порошка или гранул в качестве реагента, понижающего уровень рН в бассейнах
Получение
Если взять только 1 моль основания — то есть меньше, чем требуется для полной нейтрализации, то образуется кислая соль — гидросульфит натрия:
Физические свойстваПравить
- Гидросульфат натрия образует бесцветные кристаллы триклинной сингонии, пространственная группа P , параметры ячейки = 0,7005 нм, = 0,7125 нм, = 0,6720 нм, = 95,93°, = 92,31°, = 75,52°, . При нагревании претерпевает два полиморфных перехода при 140 и 170 °C.
- Кристаллогидрат гидросульфата натрия — бесцветные гигроскопические кристаллы моноклинной сингонии, пространственная группа A a, параметры ячейки = 0,8213 нм, = 0,7812 нм, = 0,7805 нм, = 120,04°, .
Разложение бертолетовой соли
Бертолетова соль или хлорат калия разлагается на разные продукты в зависимости от условий. При нагревании до 150-300ºС в присутствие катализатора образуется хлорид калия и кислород:
- 2KClO3 → 2KCl + 3O2↑
Сходным образом разлагается перхлорат калия:
- KClO4 → KCl + 2O2↑
При температуре 400ºС бертолетова соль разлагается на перхлорат калия и хлорид калия:
- 4KClO3 → 3KClO4 + KCl
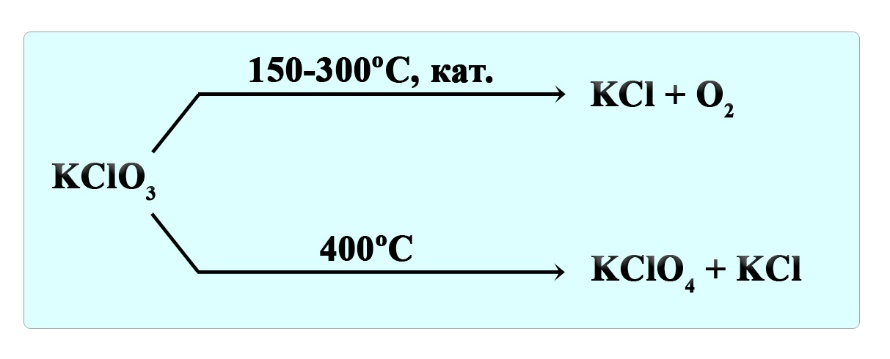
Флэш-карточки с разложением солей. Перед Вами лицевая сторона карточки с формулой соли, попробуйте вспомнить основные продукты разложения этой соли и нажмите на карточку, чтобы проверить реакцию:
Способ получения
1. В результате взаимодействия холодной и концентрированной серной кислоты и гидроксида натрия, образуется гидросульфат натрия и вода:
2. Твердый сульфат натрия реагирует с концентрированной серной кислотой. В результате реакции образуется гидросульфат натрия:
3. При температуре до 50º C в результате реакции между твердым хлоридом натрия и концентрированной серной кислотой происходит образование гидросульфата натрия и газа хлороводорода:
Химические свойства
1. Гидросульфат натрия разлагается при температуре 250–320º C в вакууме с образованием пиросульфата натрия и воды :
2. Гидросульфат натрия может взаимодействовать со сложными веществами :
2.1. Г идросульфат натрия реагирует с концентрированным раствором гидроксида натрия . При этом образуются сульфат натрия и вода:
2.2. С хлоридом натрия гидросульфат натрия реагирует при температуре 450–800º C с образованием сульфата натрия и хлороводородной кислоты:
3. Гидросульфат натрия может взаимодействовать с простыми веществами-металлами :
Например , раствор гидросульфата реагирует с цинком:
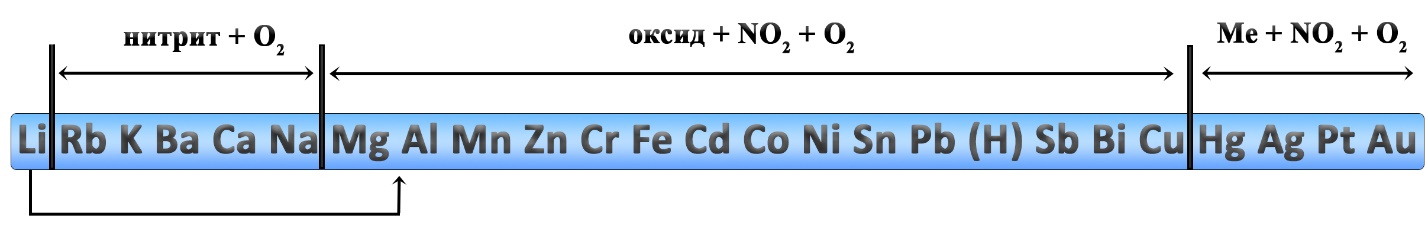
Разложение нитратов
При установлении продуктов термического разложения нитратов удобно пользоваться рядом активности металлов, однако к нему следует добавить некоторые уточнения: литий и магний, обычно относятся к активным металлам, но разложение нитратов этих двух металлов происходит как у металлов средней активности. Медь относится к неактивным металлам, но разложение нитрата меди II идёт как разложение нитрата металла средней активности. Данные реакции являются весьма популярными в химии. На ЕГЭ задачи по разложению нитратов встречаются в заданиях линии 7 и 31.
Уравнения разложения нитратов активных металлов (кроме лития и магния):
- 2KNO3 → 2KNO2 + O2↑ ‒ разложение нитрата калия
- 2NaNO3 → 2NaNO2 + O2↑ ‒ разложение нитрата натрия
- 2CsNO3 → 2CsNO2 + O2↑ ‒ разложение нитрата цезия
- 2RbNO3 → 2RbNO2 + O2↑ ‒ разложение нитрата рубидия
- Ca(NO3)2 → Ca(NO2)2 + O2↑ ‒ разложение нитрата кальция
- Ba(NO3)2 → Ba(NO2)2 + O2↑ ‒ разложение нитрата бария
- Sr(NO3)2 → Sr(NO2)2 + O2↑ ‒ разложение нитрата стронция
Уравнения разложения нитратов металлов средней активности, нитрата лития и нитрата меди II:
- 4LiNO3 → 2Li2O + 4NO2↑ + O2↑ ‒ разложение нитрата лития
- 2Mg(NO3)2 → 2MgO + 4NO2↑ + O2↑ ‒ разложение нитрата магния
- 2Zn(NO3)2 → 2ZnO + 4NO2↑ + O2↑ ‒ разложение нитрата цинка
- 2Cu(NO3)2 → 2CuO + 4NO2↑ + O2↑ ‒ разложение нитрата меди II
- 4Al(NO3)3 → 2Al2O3 + 12NO2↑ + 3O2↑ ‒ разложение нитрата алюминия
- 4Fe(NO3)3 → 2Fe2O3 + 12NO2↑ + 3O2↑ ‒ разложение нитрата железа III
- 4Cr(NO3)3 → 2Cr2O3 + 12NO2↑ + 3O2↑ ‒ разложение нитрата хрома III
Во всех приведенных реакциях степень окисления металла не изменяется. Это характерно для нитратов, содержащих металл в высшей или наиболее устойчивой степени окисления. Если же нитрат образован переходным металлом в низшей степени окисления, то при разложении этого нитрата происходит окисление еще и металла.
Разложение кислот
Неустойчивыми кислотами являются угольная, сернистая кислота и азотистая кислота, они разлагаются даже при небольшом нагревании:
- H2CO3 → CO2↑ + H2O ‒ разложение угольной кислоты
- H2SO3 → SO2↑ + H2O ‒ разложение сернистой кислоты
- 2HNO2 → NO↑ + NO2↑ + H2O ‒ разложение азотистой кислоты без нагревания
- 3HNO2 → HNO3 + 2NO↑ + H2O – разложение азотистой кислоты при нагревании
Разложение остальных кислот требует нагревания:
- 4HNO3 → 4NO2 + O2↑ + 2H2O ‒ разложение азотной кислоты
- H2SiO3 → SiO2 + H2O – разложение кремниевой кислоты
Уравнения реакций разложения комплексных солей
При нагревании комплексные соли теряют воду, превращаясь в средние соли, степени окисления при этом не изменяются:
- Na[Al(OH)4] → NaAlO2 + 2H2O↑ ‒ разложение тетрагидроксоалюмината натрия
- K2[Zn(OH)4] → K2ZnO2 + 2H2O↑ ‒ разложение тетрагидроксоцинката калия
- Ca[Be(OH)4] → CaBeO2 + 2H2O↑ ‒ разложение тетрагидроксобериллата кальция
- Ba[Al(OH)4]2 → Ba(AlO2)2 + 4H2O↑ ‒ разложение тетрагидроксоалюмината бария
Гидросульфит натрия. Физические и химические свойства. Применение
Гидросульфит натрия – это неорганическое соединение, соль кислая металла натрия и сернистой кислоты, консервант (Е222) и антиоксидант. Обладает отбеливающими свойствами. Имеет следующую химическую формулу: NaHSO3.
Физические свойства гидросульфита натрия:
1. Представляет собой порошок белого цвета, имеющий слабый сероватый оттенок.
2. Молярная масса составляет 104.061 грамм/моль, плотность – 1.48 грамм/сантиметр³.
3. Температура плавления равна 150 градусам по Цельсию.
4. Хорошо растворяется в воде (H2O) и в разбавленных щелочах.
Химические свойства натрия гидроксида:
1. Разлагается при нагревании:
2NaHSO3 (натрия гидросульфит) = Na2SO3 (натрия сульфит) + SO2 (сернистый газ, выделяется в виде газа) + H2O (вода)
2. Разлагается кислотами:
NaHSO3 + HCl (соляная кислота) = NaCl (натрия хлорид) + SO2 (сернистый газ) + H2O (вода)
3. Разлагается щелочами:
NaHSO3 + NaOH (гидроксид) = Na2SO3 (натрия сульфит) + H2O (вода)
4. Окисляется кислородом:
4NaHSO3 + O2 = 2Na2SO4 (сульфат натрия) + 2SO2 (сернистый газ, улетучивается)+ H2O (вода)
Как получают гидросульфит натрия?
Данное вещество можно получить следующими способами:
1. Путем взаимодействия гидроксида натрия с оксидом серы:
NaOH (натрия основание) + SO2 (оксид серы) = NaHSO3 (натрия гидросульфит)
2. Посредством реакции (при комнатной температуре) дитионита натрия с водой и соляной кислотой:
2Na2S2O4 (натрия дитионит) + H2O (вода) + HCl (соляная кислота) = 2NaHSO3 (натрия гидросульфит) + S (сера, выпадает в виде осадка) + NaCl (натриевый хлорид)
3. При помощи реакции, в которой взаимодействует дитионит натрия, вода и кислород:
2Na2S2O4 (дитионит натрия в разбавленной виде) + 2H2O (вода) + O2 (кислород) = 4NaHSO3 (гидросульфит натрия)
Применение гидросульфита натрия:
— легкая, химическая и другие отрасли промышленности;
— в пищевой промышленности используется как антиокислитель или консервант;
— применяется почти во всех винах, идущих на экспорт (химические свойства натрия гидросульфита в этом случае помогают предотвратить окисление и сохранить вкус напитка);
— применяется при консервировании фруктов для борьбы с микробами и предотвращения потемнения;
— при крашении и белении различных тканей используется как консервирующее средство;
— для снятия активных красителей в процессе крашения хлопка;
— при крашении полиэфиров для восстановительной очистки;
— как консервирующее средство при отбеливании тканей и как восстановитель для кубовых красителей;
— в биохимической инженерии используется в целях поддержания анаэробных условий в реакторе.
Токсичен ли гидросульфит натрия для человека?
Рассматриваемое нами вещество в чрезмерных концентрациях может стать причиной серьезных аллергических реакций. С тысяча девятьсот восьмидесятого года NaHSO3 (как и гидросульфит калия, Е 228) запрещен в Соединенных Штатах Америки к использованию на сырых фруктах и овощах после ряда случаев летального исхода. Гидросульфит натрия вызывает различные недуги пищеварительной системы. Согласно директиве Евросоюза о веществах, представляющих опасность для человека, добавка Е 222 относится к группе опасных химических соединений. В Украине и Российской Федерации данное вещество разрешено к использованию только со строгим соблюдением технологий.
Использование гидросульфата натрия в пищевой промышленности
Данное вещество в пищевой промышленности используется под названием Е 222. Это пищевая добавка синтетического происхождения, имеющая высокий уровень опасности. При долгом систематическом употреблении наносит серьезный вред организму. Благодаря свойству угнетать размножение и рост микроорганизмов и бактерий используется в качестве антиоксиданта и консерванта. В кислой среде гидросульфит натрия разлагается на серосодержащие соединения и саму серу.
Меры первой помощи при отравлениях
Рекомендуется покой и тепло, сухая и чистая одежда, а также свежий воздух. Кожу и глаза необходимо промыть прохладной водой. При ожогах надо наложить асептическую повязку. Далее вызвать скорую помощь.
Особые реакции разложения нитратов
Разложение нитрата железа II:
- 4Fe(NO3)2 → 2Fe2O3 + 8NO2↑ + O2↑
В данной реакции два восстановителя – железа поднимает степень окисления с +2 до +3, кислород с ‒2 до 0. Окислитель – азот +5.
Аналогично идет реакция термического разложения нитрата хрома II:
- 4Cr(NO3)2 → 2Cr2O3 + 8NO2↑ + O2↑
Разложение нитрата марганца II идет иначе, так как для марганца следующей после +2 устойчивой степенью окисления является не +3, а +4:
- Mn(NO3)2 → MnO2 + 2NO2↑
Обратите внимание на то, что кислород в этой реакции не выделяется!
Задание в формате ЕГЭ с ответом:
Установите соответствие между названием вещества и продуктами его разложения: к каждой позиции, обозначенной буквой подберите позицию, обозначенную цифрой.
- нитрат железа II
- нитрат меди II
- нитрат ртути II
- нитрат магния
- нитрат калия
- нитрат серебра
- MeNO2 + O2
- MeO + NO2 + O2
- Me + NO2 + O2
- Me2O3 + NO2 + O2
Пример задания из КИМ ЕГЭ:
Установите соответствие между формулой вещества и продуктами его разложения: к каждой позиции, обозначенной буквой подберите позицию, обозначенную цифрой.
- LiNO3
- Cu(NO3)2
- RbNO2
- Zn(NO3)2
- Hg(NO3)2
- Al(NO2)3
- MeNO2 + O2
- MeO + NO2 + O2
- Me + NO2 + O2
- Me2O + NO2 + O2
- Me2O3 + NO2 + O2
Разложение нитрата аммония будет рассмотрено ниже, в реакциях разложения солей аммония.
Разложение гидроксидов
Еще одна популярная тема в разложении веществ – термическое разложение гидроксидов. Большинство нерастворимых гидроксидов неустойчивы, разлагаются на оксид и воду. При этом степень окисления металла не меняется. Растворимые гидроксиды (щелочи) не разлагаются, за исключением неустойчивого гидроксида аммония (который не является щелочью).
- 2Al(OH)3 → Al2O3 + 3H2O ‒ разложение гидроксида алюминия
- Zn(OH)2 → ZnO + H2O ‒ разложение гидроксида цинка
- Cu(OH)2 → CuO + H2O ‒ разложение гидроксида меди II
- 2Fe(OH)3 → Fe2O3 + 3H2O ‒ разложение гидроксида железа III
- NH4OH → NH3↑ + H2O или NH3·H2O → NH3↑ + H2O ‒ разложение гидроксида аммония
Разложение гидросульфитов
Идет сходным с разложением гидрокарбонатов образом, при термическом размножении этих солеи образуются сульфиты и выделяется газ:
- 2KHSO3 → K2SO3 + SO2↑ + H2O↑ ‒ разложение гидросульфита калия
- Ba(HSO3)2 → BaSO3 + SO2↑ + H2O↑ ‒ разложение гидросульфита бария
Разложение карбонатов
Реакции разложения карбонатов также происходит при нагревании. Карбонаты щелочных металлов (IА-группа), кроме карбоната лития, не разлагаются. Большинство других карбонатов разлагаются до оксидов, карбонат серебра и карбонат ртути разлагаются с выделением свободного металла.
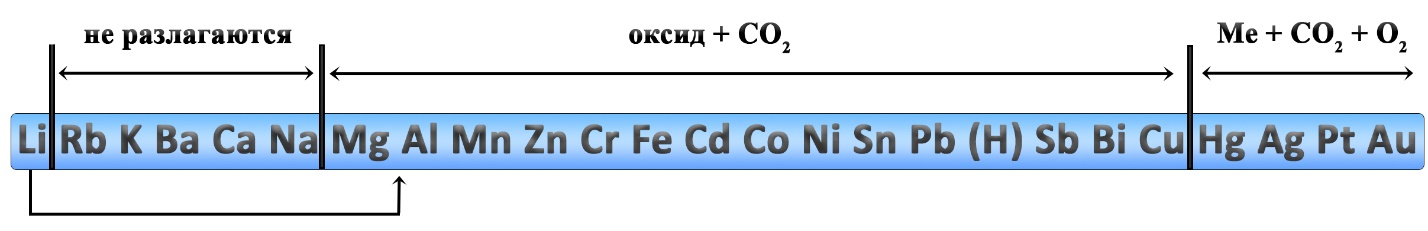
- Li2CO3 → Li2O + CO2↑ ‒ разложение карбоната лития
- MgCO3 → MgO + CO2↑ ‒ разложение карбоната магния
- CaCO3 → CaO + CO2↑ ‒ разложение карбоната кальция
- CuCO3 → CuO + CO2↑ ‒ разложение карбоната меди II
- 2HgCO3 → 2Hg + 2CO2↑ + O2↑ ‒ разложение карбоната ртути II
- 2Ag2CO3 → 4Ag + 2CO2↑ + O2↑ ‒ разложение карбоната серебра
Какие из перечисленных карбонатов разлагаются?
- Na2CO2
- MgCO3
- CaCO3
- K2CO3
- Cs2CO3
- CuCO3
При разложении каких карбонатов образуется оксид металла?
- Na2CO3
- HgCO3
- Li2CO3
- CaCO3
- Ag2CO3
- FeCO3
При нагревании образца гидросульфита натрия часть вещества разложилась
При нагревании образца гидросульфита натрия часть вещества разложилась. При этом выделилось 448 мл (н. у.) сернистого газа и образовалось 5,64 г твёрдого безводного остатка. Остаток добавили к 0,855 %-ному раствору гидроксида бария. При этом в полученном растворе не осталось ни ионов бария, ни сульфит-анионов. Определите массовую долю гидроксида натрия в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
1) Уравнения реакций:
$2NaHSO_3 = Na_2SO_3 + H_2O + SO_2↑$ (1)
$Na_2SO_3 + Ba(OH)_2 = BaSO_3↓ + 2NaOH$ (2)
$NaHSO_3 + Ba(OH)_2 = BaSO_3↓ + NaOH + H_2O$ (3)
Формула для вычисления массовой доли KOH:
2) $n(SO_2)_<(1)>$ = 0.448 / 22.4 = 0.02 моль
3) По уравнению (1):
$n(Na_2SO_3) = n(SO_2)$ = 0.02 моль
$M(Na_2SO_3)$ = 138 г/моль, $m(Na_2SO_3)$ = 0.02 · 126 = 2.52 г
4) Находим количество непрореагировавшего $NaHSO_3$:
$m(NaHSO_3)_<не прореаг.>$ = 5.64 – 2.52 = 3,12 г
$M(NaHSO_3)$ = 104 г/моль, $n(NaHSO_3)$ = 3.12 / 104 = 0.03 моль
5) По уравнениям (2) и (3):
$n(Ba(OH)_2)_ <(2)>= n(Na_2SO_3)$ = 0.02 моль
$n(Ba(OH)_2)_ <(3)>= n(NaHSO_3)$ = 0.03 моль
$n(Ba(OH)_2)_<общее>$ = 0.02 + 0.03 = 0.05 моль
$M(Ba(OH)_2)$ = 171 г/моль; $m(Ba(OH)_2)_<общая>$ = 0.05 · 171 = 8.55 г
$m_<р-ра>(Ba(OH)_2)$ = 8.55 / 0.00855 = 1000 г
6) По уравнениям (2) и (3):
$n(BaSO_3)_ <(2)>= n(Na_2SO_3)$ = 0.02 моль
$n(BaSO_3)_ <(3)>= n(NaHSO_3)$ = 0.03 моль
$n(BaSO_3)_<общее>$ = 0.02 + 0.03 = 0.05 моль
$M(BaSO_3)$ = 217 г/моль; $m(BaSO_3)$ = 0.05 · 217 = 10.85 г
7) По уравнениям (2) и (3):
$n(NaOH)_ <(2)>= 2n(Na_2SO_3)$ = 2 ∙ 0.02 = 0.04 моль
$n(NaOH)_ <(3)>= n(NaHSO_3)$ = 0.03 моль
$n(NaOH)_<общее>$ = 0.04 + 0.03 = 0.07 моль
M(NaOH) = 40 г/моль, m(NaOH) = 0.07 · 40 = 2.8 г
8) $m_<р-ра>(NaOH)$ = 5.64 + 1000 – 10.85 = 994.79 г
9) ω(NaOH) = 2.8 / 994.79 ≈ 0.0028. или 0.28 %
Гидросульфат натрия
- Гидросульфат натрия
Гидросульфат натрия — кислая соль натрия и серной кислоты с формулой NaHSO4, бесцветные кристаллы. Образует кристаллогидрат NaHSO4•H2O.
- Гидросульфат натрия получают действием избытка концентрированной серной кислоты на едкий натр:
- Гидросульфат натрия образует бесцветные кристаллы триклинной сингонии, пространственная группа P , параметры ячейки a = 0,7005 нм, b = 0,7125 нм, c = 0,6720 нм, α = 95,93, β = 92,31, γ = 75,52, Z = 4. При нагревании претерпевает два полиморфных перехода при 140 и 170°С.
- Кристаллогидрат гидросульфата натрия — бесцветные гигроскопические кристаллы моноклинной сингонии, пространственная группа A a, параметры ячейки a = 0,8213 нм, b = 0,7812 нм, c = 0,7805 нм, β = 120,04, Z = 4
- При подщелачивании гидросульфат натрия переходит в сульфат:
- При спекании гидросульфат натрия взаимодействует с солями:
- Как флюс в цветной металлургии.
- Как реагент для перевода труднорастворимых окислов в растворимые сульфаты.
- Зарегистрирован в качестве пищевой добавки E514.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — .: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — .: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — : Химия, 1971. — Т. 2. — 1168 с.
- Соединения натрия
- Сульфаты
- Неорганические вещества
.
.
Смотреть что такое “Гидросульфат натрия” в других словарях:
Разложение сульфатов
Сульфаты щелочных металлов не разлагаются при нагревании. Сульфаты серебра и ртути разлагаются до свободного металла, сульфаты остальных металлов разлагаются до оксида металла, сернистого газа и кислорода.
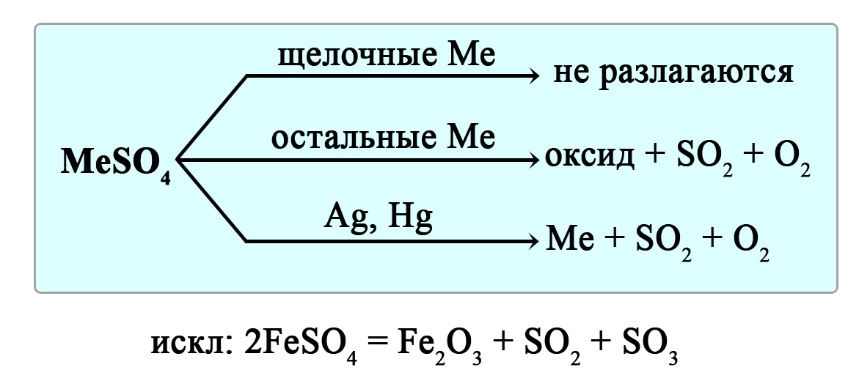
Уравнения реакция разложения сульфатов:
- 2CaSO4 → 2CaO + 2SO2↑ + O2↑ ‒ реакция разложения сульфата кальция
- Ag2SO4 → 2Ag + 2SO2↑ + O2↑ ‒ реакция разложения сульфата серебра
Реакция разложения дихромата калия и перманганата калия
На ЕГЭ по химии реакции разложения дихромата калия и перманганата калия часто встречаются в заданиях линии 29 и 31.Эти две реакции похожи, поэтому их удобно запоминать сразу парой:
- 4K2Cr2O7 → 4K2CrO4 + 2Cr2O3 + 3O2↑ ‒ уравнение термического разложения дихромата калия
- 2KMnO4 → K2MnO4 + MnO2 + O2↑ ‒ уравнение термического разложение перманганата калия
Гидросульфат натрия
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 22 июля 2018 года; проверки требуют 10 правок.
Гидросульфа́т на́трия — кислая соль натрия и серной кислоты с формулой NaHSO4, бесцветные кристаллы.
Образует кристаллогидрат NaHSO4·H2O.
Разложение органических веществ
Сходным образом происходит и разложение органических веществ – гидроксидов метиламмония, диметиламмония, триметиламмония и некоторых других.
- [CH3-NH3]OH → CH3-NH2↑ + H2O ‒ разложение гидроксида метиламмония
- [(CH3)2-NH2]OH → (CH3)2-NH↑ + H2O ‒ разложение гидроксида диметиламмония
- [(CH3)3-NH]OH → (CH3)3-N↑ + H2O ‒ разложение гидроксида триметиламмония
Разложение веществ
Материал по химии
Свойства
Обладает отбеливающими свойствами; хорошо растворим в воде.
Применение
Натрия гидросульфит применяют в легкой, химической и других отраслях промышленности. В пищевой промышленности применяется как консервант или антиокислитель.
Гидросульфит натрия используется почти во всех идущих на экспорт винах для предотвращения окисления и сохранения вкуса. При консервировании фруктов применяется для предотвращения потемнения и для борьбы с микробами. В очень больших концентрациях может вызывать серьёзные аллергические реакции. Используется как консервирующее средство, при белении и крашении тканей.
Разложение солей аммония
При разложении солей аммония чаще всего образуется аммиак, исключения составляют соли, в которых анион проявляет окислительные свойства. Например, хлорид, бромид, йодид, сульфиды, карбонаты и фосфаты разлагаются без изменения степеней окисления (без ОВР). Процессы идут при нагревании:
- NH4Cl → NH3↑ + HCl↑ ‒ разложение хлорида аммония
- NH4Br → NH3↑ + HBr↑ ‒ разложение бромида аммония
- NH4I → NH3↑ + HI↑ ‒ разложение йодида аммония
- (NH4)2S → 2NH3↑ + H2S↑ ‒ разложение сульфида аммония
- NH4HS → NH3↑ + H2S↑ ‒ разложение гидросульфида аммония
- (NH4)3PO4 → 3NH3↑ + H3PO4 ‒ разложение фосфата аммония
- (NH4)2HPO4 → 2NH3↑ + H3PO4 ‒ разложение гидрофосфата аммония
- NH4H2PO4 → NH3↑ + H3PO4 ‒ разложение дигидрофосфата аммония
- (NH4)2CO3 → 2NH3↑ + CO2↑ + H2O↑ ‒ разложение карбоната аммония
- NH4HCO3 → NH3↑ + CO2↑ + H2O↑ ‒ разложение гидрокарбоната аммония
Разложение солей аммония с изменением степени окисления:
Разложение нитрита и нитрата аммония легко запомнить вместе, отнимите от этих солей всю воду и получите нужный продукт:
- NH4NO3 → 2H2O + N2O ‒ разложение нитрата аммония
- NH4NO2 → 2H2O + N2 ‒ разложение нитрита аммония
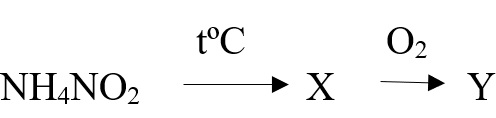
Задание по образцу ФИПИ:
Задана следующая схема превращений веществ. Определите, какие из указанных веществ являются веществами X и Y. В ответ запишите соответствующую последовательность цифр без пробелов и дополнительных знаков, сначала вещество Х, затем вещество Y.
- NH3
- NH4NO3
- N2O
Азот окисляется до NO
Удобно запоминать вместе и разложение дихромата и перманганата аммония, так как образуются сходные продукты – азот, оксид и соль:
- (NH4)2Cr2O7 → N2↑ + Cr2O3 + 4H2O↑ ‒ разложение дихромата аммония
- 2NH4MnO4 → N2↑ + 2MnO2 + 4H2O↑ ‒ разложение перманганата аммония
Попробуйте решить задание ЕГЭ:
Установите соответствие между названием вещества и продуктами его разложения: к каждой позиции, обозначенной буквой подберите позицию, обозначенную цифрой.
- нитрит аммония
- нитрат аммония
- дихромат аммония
- хлорид аммония
- N2 + Cr2O3 + H2O
- NH3 + Cl2 + H2
- N2 + H2O
- NO2 + Cr2O3 + H2O
- NH3 + HCl
- N2O + H2O
Разложение гидрокарбонатов
Гидрокарбонаты разлагаются до соответствующих карбонатов:
- 2NaHCO3 → Na2CO3 + CO2↑ + H2O↑ ‒ разложение гидрокарбоната натрия
- Ca(HCO3)2 → CaCO3 + CO2↑ + H2O↑ ‒ разложение гидрокарбоната кальция
При длительном нагревании происходит более глубокое разложение (это не качается гидрокарбонатов щелочных металлов, они в любом случае остаются карбонатами).
Например, в некоторых задачах может встретиться следующая фраза «гидрокарбонат нагревали до постоянной массы» или «смесь гидрокарбоната и карбоната нагревали до постоянной массы», какие реакции следует указать?
Если нагревают гидрокарбонат щелочного металла, то реакция одна:
- 2KHCO3 → K2CO3 + CO2↑ + H2O↑
Если нагревают другие гидрокарбонаты, то нужно писать две реакции:
- Ba(HCO3)2 → BaCO3 + CO2↑ + H2O↑ ‒ нагревание
- BaCO3 → BaO + CO2↑ ‒ при продолжении нагревания
ПолучениеПравить
- Гидросульфат натрия получают действием серной кислоты на гидроксид или сульфат натрия:
Разложение сульфитов
В отличие от реакция термического разложения карбонатов, большинство сульфитов разлагаются при нагревании со сменой степени окисления (происходит реакция самоокисления-самовосстановления или диспропорционирования). При нагревании сульфита образуется смесь сульфидов и сульфатов:
- 4Na2SO3 → 3Na2SO4 + Na2S ‒ термическое разложение сульфита натрия
- 4CaSO3 → 3CaSO4 + CaS ‒ термическое разложение сульфита кальция
Также
- Тетраалкиаммониевые соли (формула NR4HSO3)
Реакции разложения солей
Термическому разложению подвергаются многие соли – карбонаты, нитраты, нитриты, сульфаты, кислые, основные и комплексные соли. Рассмотрим наиболее популярные уравнения разложения солей. Разложение солей часто встречается в ЕГЭ по химии в линии заданий 31, это задание считается одним из самых сложных заданий экзамена.
Способы получения и химические свойства
Гидросульфат натрия NaHSO4 — кислая соль щелочного металла натрия и серной кислоты. Белое кристаллическое вещество. Плавится без разложения, при дальнейшем нагревании разлагается.
Относительная молекулярная масса Mr = 120,06; относительная плотность для ж. и тв. состояния d = 2,742; tпл = 186º C;
Химические свойстваПравить
- При подщелачивании гидросульфат натрия переходит в сульфат:
- При спекании гидросульфат натрия взаимодействует с солями:
- и оксидами: