Работа с карточками маркируемых товаров
Программа для маркировки товаров в 1С – ХамелеонЦРПТ предназначена для взаимодействия с различными структурами контролирующими процесс товарооборота на территории РФ, основными сущностями в процессе взаимодействия которого являются:
GTIN (Global Trade Item Number) – глобальный номер товарной продукции в единой международной базе товаров GS1.
Карточка товара – определенный международными регламентами набор данных, хранящийся в Национальном каталоге ГИС МТ Честный знак.
1 Получение GTIN в GS1
Вам потребуется следующая информация о товаре:
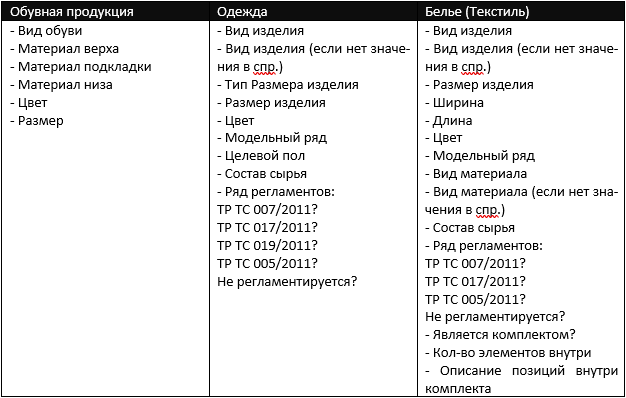
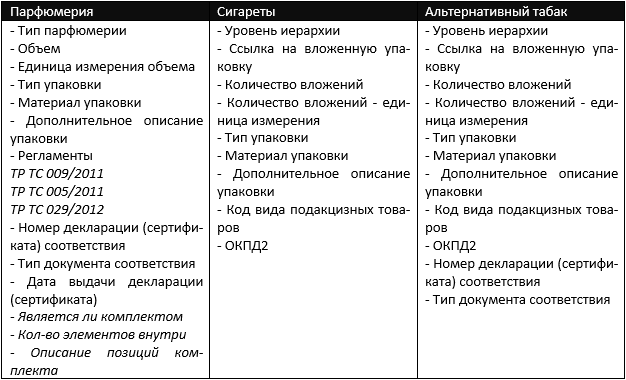

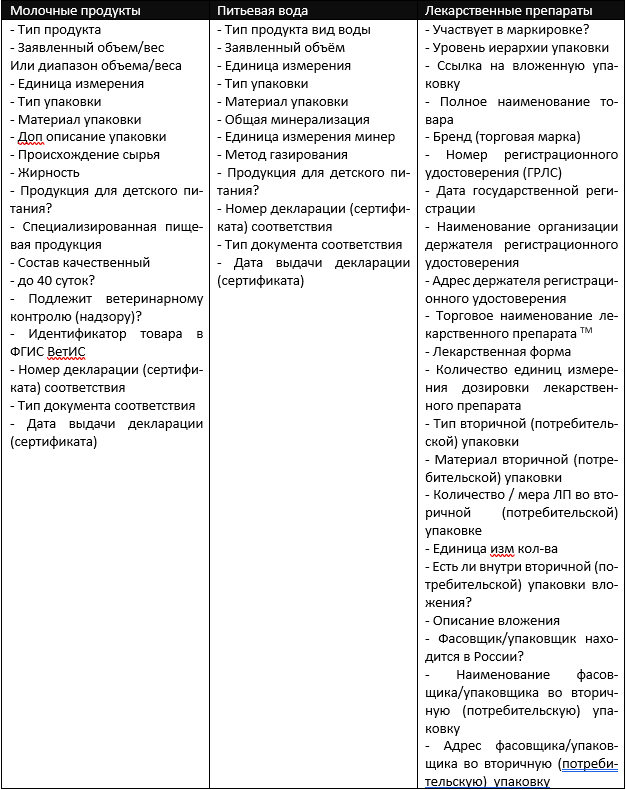
Если до начала использования программы Хамелеон ЦРПТ заказ GTIN уже производился, то можно произвести загрузку ранее полученных GTIN в базу данных системы.
Функция доступна по нажатию кнопки:
Действия/На основании – Перечитать данные из архива GS1.
1 Заполнение информации о товаре в шаблоне.
Существует несколько способов заполнения шаблона заявки на получение GTIN.
1 Заполнение шаблона заказа GTIN вручную, предоставляемого сервисом GS1.
Данный способ рекомендуется при формировании заявок на небольшое количество заказываемых GTIN номеров.
При формировании большого списка новых карточек товаров (например, при маркировке остатков по полной схеме атрибутивного состава) воспользуйтесь любым удобным способом из предыдущих пунктов.
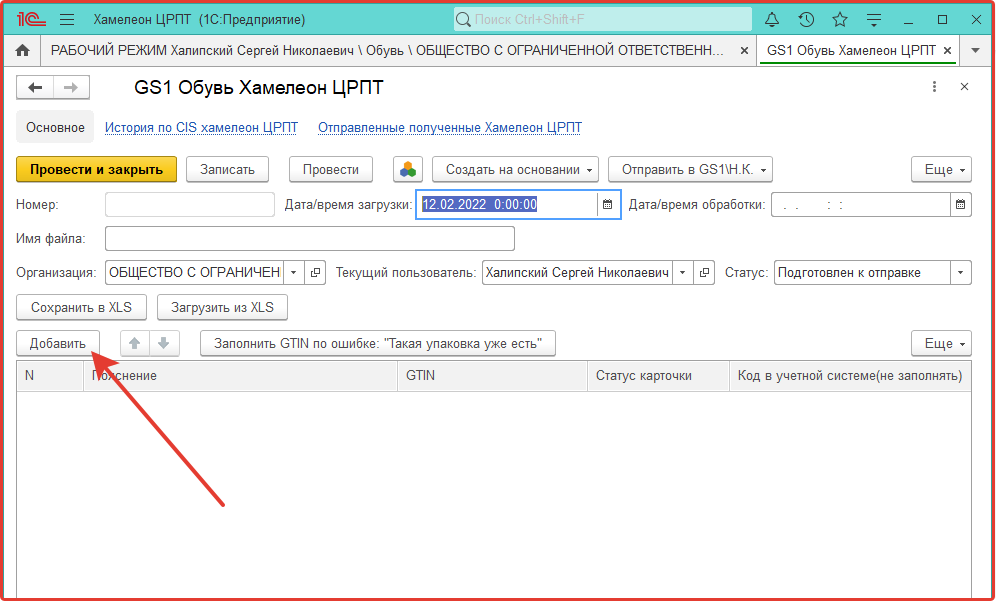
На вкладке «Получение GTIN в GS1» нажмите кнопку Создать.
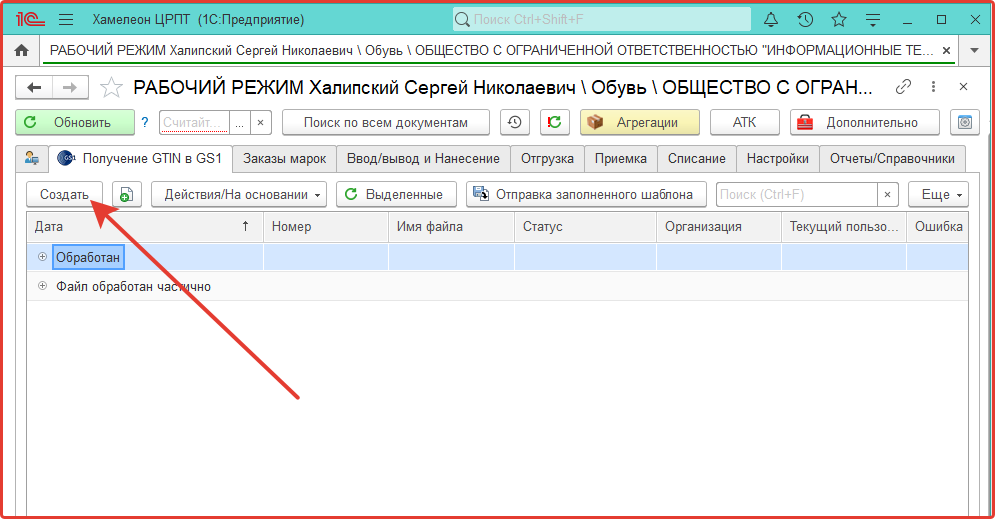
В табличной части открывшейся формы нажимаем кнопку Добавить и заполните данные в добавленной строке.
Не оставляйте строки незаполненными.
Пустые строки можно удалить нажатием клавиши Delete.
2 Отправка заявки посредством системы Хамелеон ЦРПТ
Если у вас есть заполненный шаблон заказа GTIN кодов маркировки в формате Excel (*.xlsx), его нужно загрузить в документ заказа на форме Хамелеон ЦРПТ.
Для этого воспользуйтесь кнопкой Отправка заполненного шаблона на форме списка документов
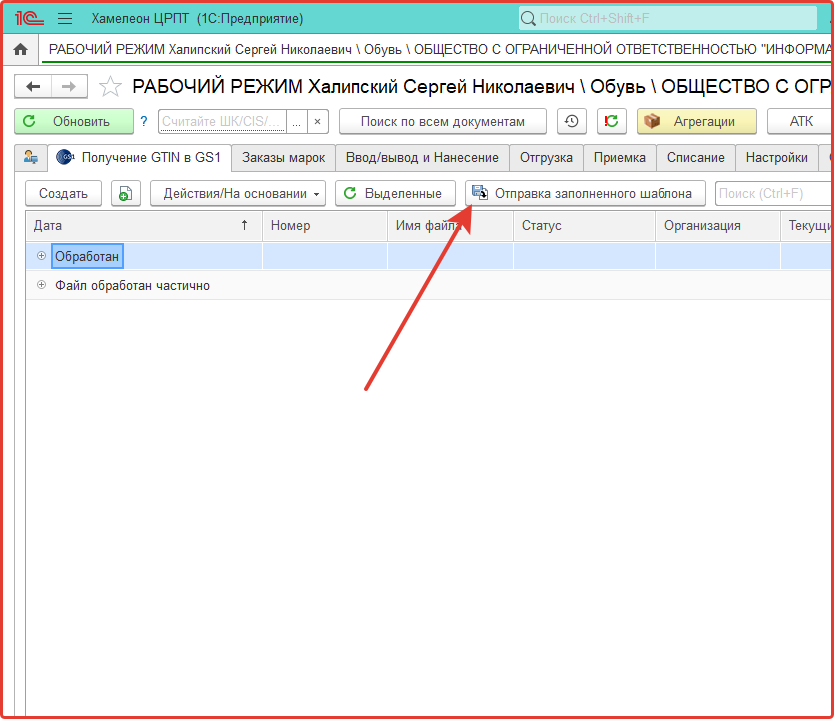
или кнопкой Загрузить из XLS в форме документа.
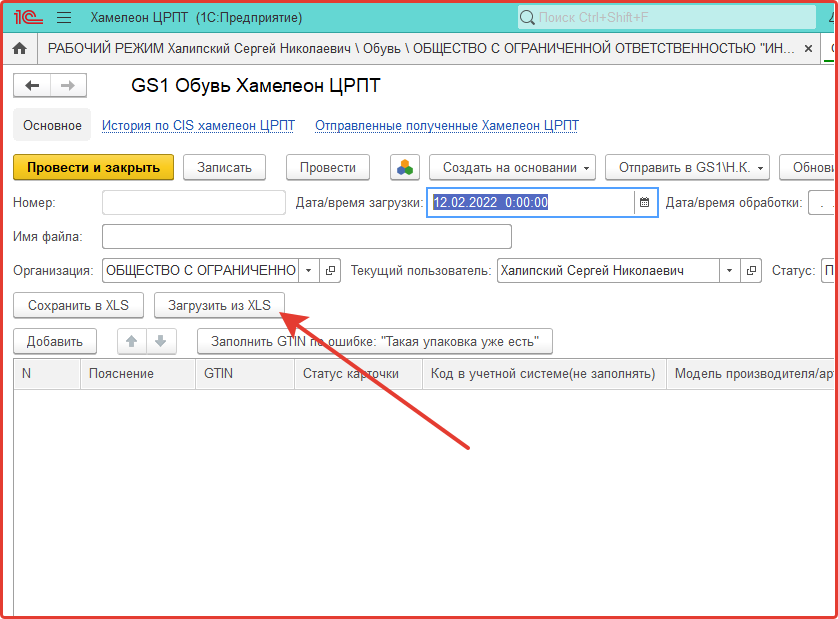
После заполнения табличной части документа заказа, его можно сохранить нажатием кнопки Записать или сразу отправить в GS1 кнопками:
Отправить в GS1/НК – Отправить в GS1.
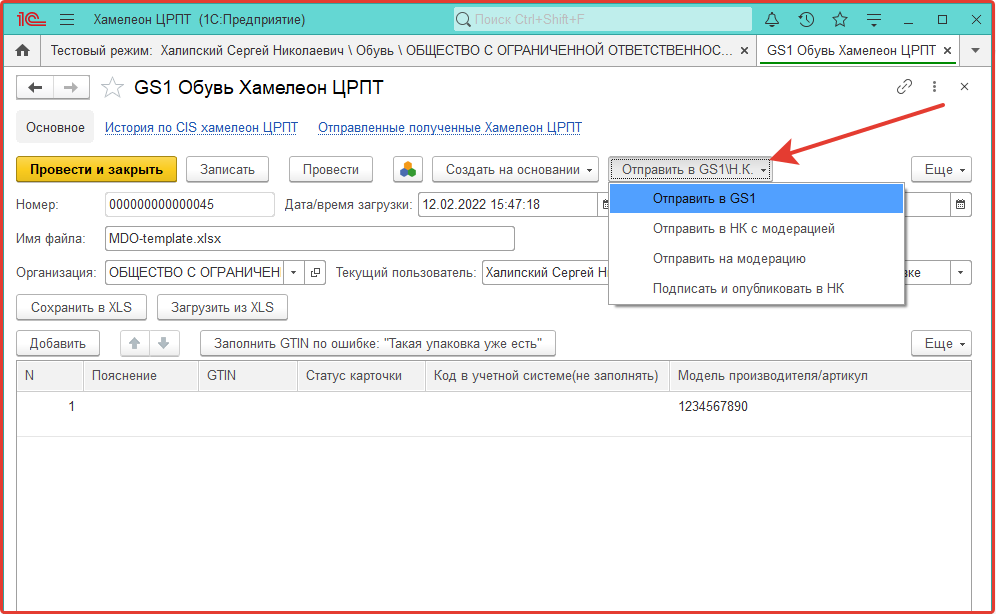
Все заявки, созданные в системе GS1 имеют определенный статус:
– Обработана частично
После обработки документа системой, у документа заказа меняется статус.
Проверка статуса документа производится выбором соответствующей строки из списка документов и нажатием кнопки:
Обновить выделенные.
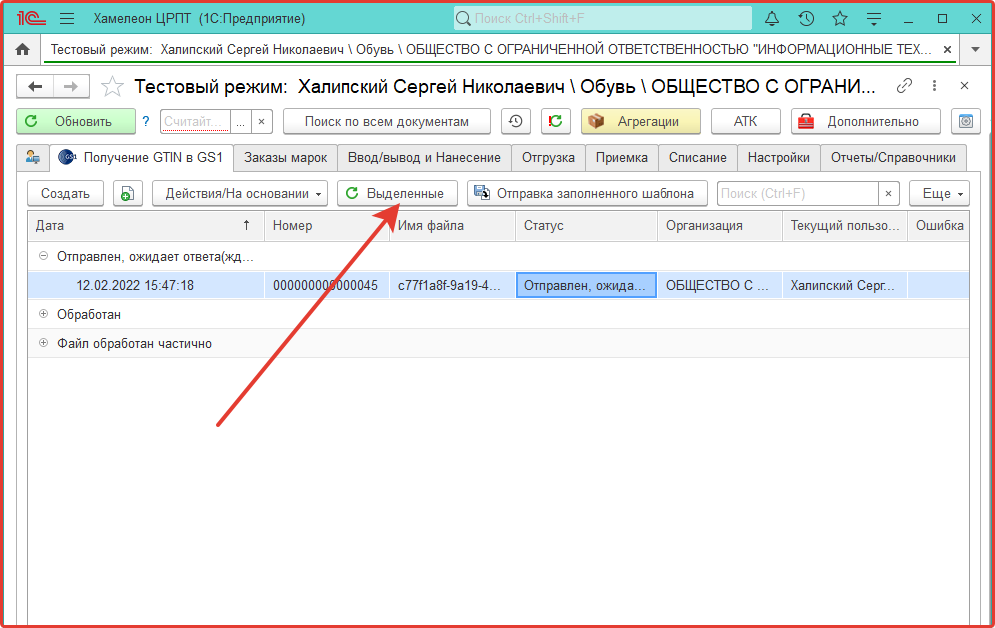
Нажатие кнопок «Обновить» или «Обновить последние 5 документов» произведут сверку каждого документа с данными на сервере GS1, если документов много то это может занять длительное время.
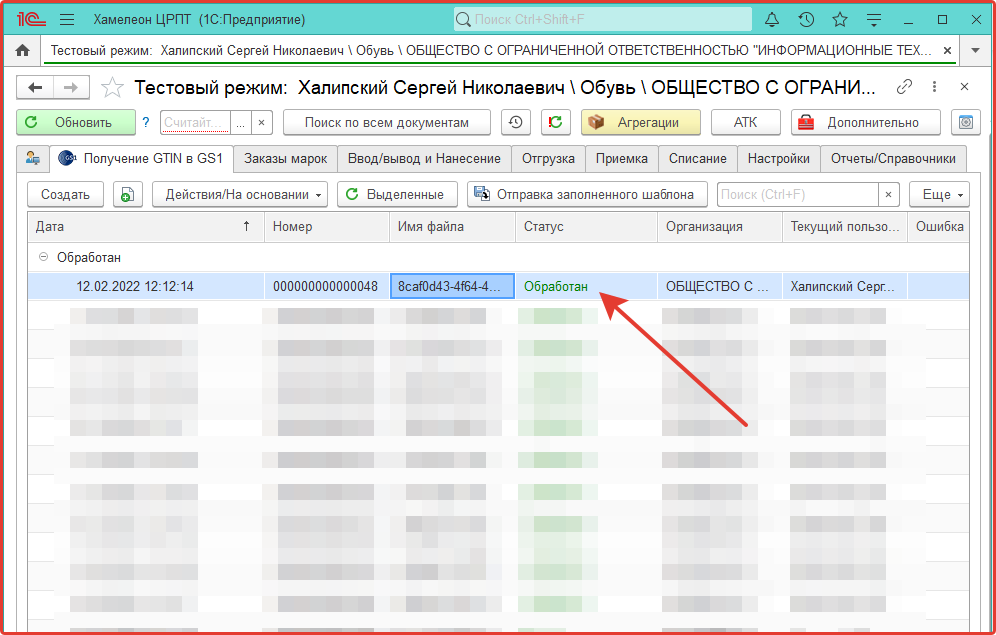
При изменении статуса документа, в последнюю колонку документа записывается результат обработки данных.
В случае выявления ошибочных данных, их можно исправить в соответствующих полях и отправить документ на повторную обработку.
В случае получения ошибки «Такая упаковка уже есть» можно заполнить поле GTIN нажатием соответствующей кнопки.
Это необходимо при создании заявки на выпуск кодов маркировки для списка товаров на основании документа заказа GTIN, так как именно это поле является ключевым при формировании КМ.

2 Работа с Национальным каталогом ГИСМТ Честный знак в Хамелеон ЦРПТ
Вся информация о товарах, для которых обязателен выпуск кодов маркировки, хранится в базе данных Честного знака – Национальном каталоге.
Информация, отражающая характеристики отдельно взятого товара, называется Карточкой товара.
В программе Хамелеон ЦРПТ карточки товаров хранятся в разделе:
Отчеты/Справочники – Список продукции.
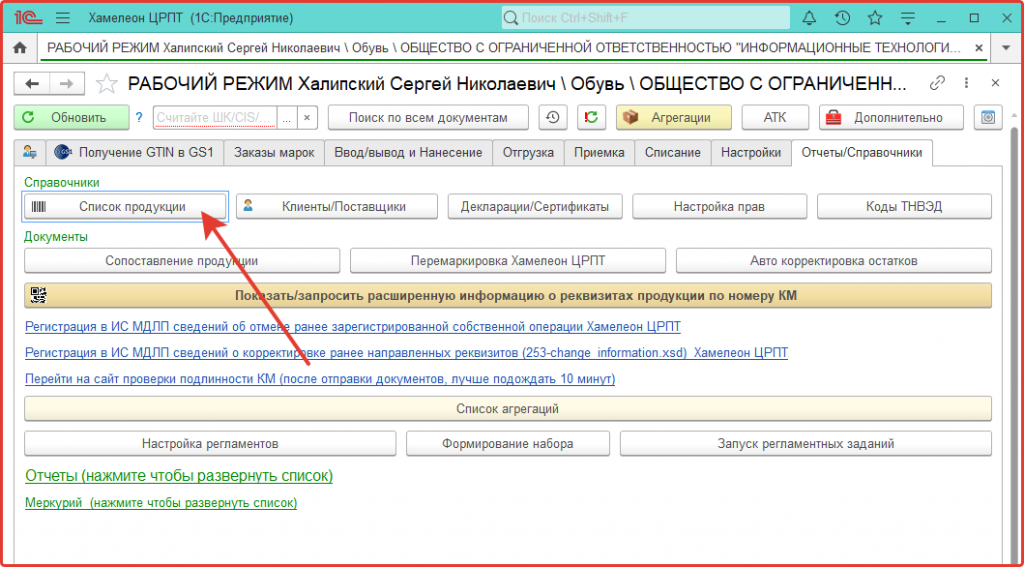
Карточки товаров загружаются из GS1 и дополняются сведениями из Национального каталога.
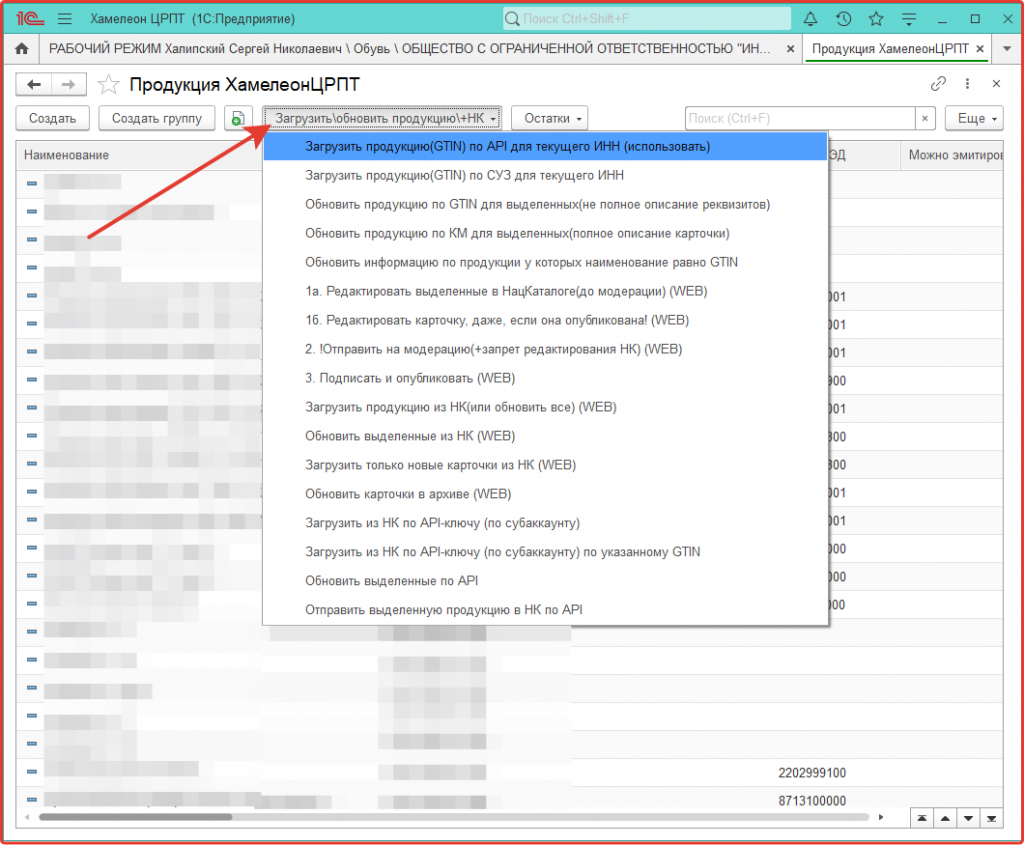
Для ручного запуска загрузки/обновления карточек товаров можно использовать кнопку:
Загрузить/Обновить продукцию с выбором требуемой операции.
Важную роль в карточке товара играет поле Статус товара в НК. Если поле пустое, значит данная карточка не синхронизирована с ГИСМТ Честный знак или отсутствует в Национальном каталоге.
В национальный каталог товар может попасть двумя способами:
– Автоматически, из системы GS1 в течении суток после успешной обработки заявки.
– Вручную, с указанием GTIN, полученным в системе GS1.
Далее будет рассмотрен ручной способ добавления.
1 Статус карточки товара «Черновик»
После добавления карточки товара в Национальный каталог она находится в статусе Черновик и не может участвовать в документах заказа марок.
В некоторых случаях, система GS1 не предоставляет всех необходимых данных для успешной модерации карточки товара.
К такому полю относится, например, значение максимальной цены на табак (за 1 пачку) в контуре Табачная продукция.
При модерации карточка с незаполненными обязательными полями уйдет в статус отказ.
В такой ситуации требуется определить обязательные для заполнения поля в форме редактирования карточки товара. Для этого заходим на сайт национального каталога, выбираем нужную группу товаров (используемый контур маркировки) и открываем карточку товара, не прошедшего модерацию.
Поля, помеченные красным цветом и есть обязательные к заполнению.
Отредактировать карточку товара можно как в самом Национальном каталоге, так и в справочнике Продукция Хамелеон ЦРПТ, после чего требуется повторная отправка карточки на модерацию соответствующими кнопками из группы кнопок:
Обновить продукцию/НК в верхней части формы.
2 Статус карточки товара «На модерации»
Карточка со статусом На модерации ожидает проверки и подтверждения модераторами ГИСМТ Честный знак.
Товары из карточки в статусе на модерации:
– Могут участвовать в документах заказа кодов маркировки.
– Не могут вводиться в оборот до смены статуса на «Опубликована».
Модерация занимает некоторое время (до трех суток), если ваша организация не переведена в режим автоматической модерации.
Подробнее об автоматической модерации можно узнать на сайте Честный знак или в технической поддержке национального каталога.
3 Статус карточки товара «Опубликована»
Когда карточка переведена в статус Опубликована, товары, на которые заказаны коды маркировки, могут вводиться в оборот. При этом дальнейшие изменения определенных полей не предусмотрены.
Данные из опубликованной карточки Национального каталога используются при проверке маркированного товара на подлинность.
4 Статус карточки товара «Требует изменений»
Если по каким-то причинам карточка товара не прошла модерацию, необходимо уточнить данные о товаре и изменить их в соответствии с требованиями Национального каталога.
Используйте справочную информацию по работе с ошибками из раздела 2.2.1 Статус карточки товара «Черновик».
3 Формирование заказа марок на основании обработанных документов заказа GTIN
Если в Национальном каталоге есть карточка товара с данным GTIN в статусе «на модерации» или «опубликована», можно оформить заказ на выпуск кодов маркировки для этого товара.
Для этого необходимо открыть обработанный документ и нажать кнопки:
Создать на основании – Заказ марок Хамелеон ЦРПТ.
Будет автоматически сформирован документ заказа КМ.
Работа с этим типом документов описана в следующем разделе.
В соответствии с положениями Федерального закона «Об обращении лекарственных средств» от 12.04.2010 N 61-ФЗ Статья 4. Основные понятия, используемые в настоящем Федеральном законе следует что:
При этом также согласно положениям статьи Статья 67. Информация о лекарственных препаратах. Система мониторинга движения лекарственных препаратов для медицинского применения также следует что:
Сам порядок урегулирован в свою очередь положениями постановления Правительства РФ от 14 декабря 2018 года N 1556 “Об утверждении Положения о системе мониторинга движения лекарственных препаратов для медицинского применения” из которых следует что:
осуществляют свою регистрацию в системе мониторинга движения лекарственных препаратов для медицинского применения
Т.е. важным вопросом в такой ситуации, является обоснованно или нет, отнесение общеобразовательных учреждения и организаций к субъектам обращения лекарственных средств, согласно положениям приведенного выше федерального законодательства, отчего и зависит выполнение обязательных требований касающихся регистрации в системе мониторинга движения лекарственных препаратов для медицинского применения.
Школа имеет лицензию на сестринское дело в педиатрии (она была необходима для получения основной лицензии на образование).
Если общеобразовательное учреждение имеет медицинскую лицензию, в рамках оказания медицинской помощи обучающимся, а такие требования в общеобразовательным учреждениям также установлены законодательством РФ, осуществляется — хранение, применение и уничтожение лекарственных средств в любом случае, иначе каким образом возможно оказывать медицинскую помощь.
А это тем самым уже является — обращением лекарственных средств, и относит общеобразовательное учреждение к — субъектам обращения лекарственных средств, которые несут обязанность по – регистрации в системе мониторинга движения лекарственных препаратов для медицинского применения.
Для чего лекарствам маркировка
По данным Всемирной организации здравоохранения, около 700 000 человек ежегодно погибают от проданных им фальсифицированных лекарств. Ни одна страна не застрахована от этой беды. Особенно развита торговля фальсифицированными противораковыми препаратами. По оценкам Всемирного экономического форума, общемировая стоимость контрафактной фармацевтической продукции в 2017 г. превысила $200 млрд.
Маркировка — это уникальный код на каждой упаковке, «паспорт» лекарства. Покупатель может считать код смартфоном и убедиться в подлинности препарата. А контролирующие органы с помощью маркировки способны отследить путь лекарства от производителя к оптовику и в точку конечной продажи. Это позволит бороться с подделками и выявлять серые схемы в обороте лекарств.
Способы перехода на маркировку лекарств
Организации и предприниматели должны отправлять в МДЛП информацию обо всех этапах движения лекарств:
Есть несколько вариантов, как выполнить все эти требования. Выбор зависит от того, есть ли у аптеки своя учетная система и насколько сложно ее менять.
Способ 1. С помощью программистов переделать свой учетный сервис или программу под маркировку.
Способ 2. Работать с маркировкой через типовую товароучетную систему.
2022
Национальная система цифровой маркировки товаров «Честный знак» будет полностью готова к началу маркировки антисептиков в соответствии с предложенными Минпромторгом России сроками. Об этом компания ЦРПТ сообщила 17 августа 2022 года. Подробнее здесь.
Мишустин утвердил постоянную упрощенную цифровую маркировку лекарств
Премьер-министр Михаил Мишустин подписал постановление, которым утвердил на постоянной основе упрощённый порядок работы в системе цифровой маркировки и прослеживания препаратов. Об этом пресс-служба Правительства РФ сообщила 10 февраля 2022 года.
Упрощенный режим работы с маркированными препаратами, вводимыми в гражданский оборот, предполагает, что производители и дистрибуторы могут реализовывать лекарства, не дожидаясь подтверждения поставщика. Сведения автоматически подтверждаются самой системой маркировки с помощью проверки кода товара и данных участников. Это дает возможность ускорить операции с препаратами для всех участников, уменьшить риски возникновения дефицита лекарств в аптеках.

Михаил Мишустин утвердил постоянную упрощенную цифровую маркировку лекарств
Такой режим временно был введен в начале ноября 2020 года, его продлевали сначала до 1 июля 2021-го, а позднее – до 1 февраля 2022 года. Теперь упрощенная схема маркировки лекарств стала постоянной.
2021
В конце декабря 2021 года премьер-министр Михаил Мишустин подписал постановление Правительства РФ, которым разрешил предоставлять фармацевтическим компаниям данные из системы маркировки. Нововведение в первую очередь предназначено для проверки контрагентов.
Согласно документу, опубликованному на официальном интернет-портале правовой информации, производители и импортеры, которые зарегистрированы в системе цифровой маркировки и прослеживания товаров «Честный знак», смогут получать от оператора системы (Центра развития перспективных технологий, ЦРПТ) информацию о текущем владельце выпущенного ими товара, количестве находящихся в обороте и проданных товаров. Также они получат доступ к сведениям о количестве проданного товара вплоть до адресов точек продаж и доступ к данным о средних розничных ценах на свои товары на уровне субъектов.

Михаил Мишустин разрешил предоставлять фармбизнесу данные из системы маркировки для проверки контрагентов
Благодаря этому бизнес сможет работать более эффективно:
Принят закон о штрафах за нарушение цифровой маркировки лекарств
26 мая 2021 года Госдума в третьем, окончательном чтении приняла закон о штрафах за нарушение требований к цифровой маркировке лекарств. Соответствующий законопроект был инициирован главой комитета Госдумы по развитию гражданского общества, вопросам общественных и религиозных объединений Сергеем Гавриловым (КПРФ).
За производство или продажу лекарств без нанесения средств идентификации будет грозить штраф: должностным лицам — 5-10 тысяч рублей, юридическим лицам — 50-100 тысяч рублей. При наложении административного штрафа препараты без маркировки будут конфисковывать.

В России принят закон о штрафах за нарушение требований к цифровой маркировки лекарств
Аналогичный размер штрафов предусмотрен за несвоевременное внесение данных в систему мониторинга движения лекарственных препаратов или за внесение в нее недостоверной информации.
Изменения вносятся в ст. 6.34 Кодекса об административных правонарушениях (КоАП) РФ. Ответственность за внесение недостоверных данных в систему мониторинга, прописанная в этой статье КоАП, сохраняется. Закон вступит в силу с 1 декабря 2021 года.
90% аптек перешли на маркировку лекарственных препаратов
К системе маркировки лекарственных препаратов планировалось перейти еще в 2020 году. Однако переход пришлось перенести. В июне 2021 года по обновленной схеме должны работать уже все аптечные пункты. Портал Pharmedu 9 февраля 2021 года опубликовал результаты опроса фармацевтов и провизоров, в котором приняли участие 5 тысяч специалистов из 6 федеральных округов России.
Респондентам был задан вопрос, готовы ли они к полноценному использованию системы маркировки и как она влияет на попадание лекарственных препаратов в аптеки.
Полностью по обновленной схеме уже работают 90% опрошенных. Более половины (65,35%) отметили, что перебои с поставками лекарств в аптеку были, но этот вопрос разрешился. Однако 32% уверяют, что проблема сохраняется.
Столько же (32%) провизоров заявили, что работать с маркировкой очень трудно, постоянно возникают те или иные проблемы. Более позитивно настроены 65% респондентов: они сообщили, что сложности есть, но работать можно. Главное неудобство, которое отметили 99% участников опроса, состоит в том, что задерживается процесс продажи, что, в свою очередь, нервирует покупателей.
Увеличения ассортимента аптеки с введением маркировки не отметил никто. А вот уменьшение подчеркнули 59,41% провизоров. Не заметили перемен 37,65%.
На вопрос, как маркировка повлияла на работу аптек, 39% ответили, что помощи от нее нет никому, но и вреда, однако, тоже никакого. Половина опрошенных разделилась во мнениях: 25% считают введение маркировки ошибкой, а другие 25% убеждены, что она помогает производителям и дистрибьютерам. А вот 13% провизоров говорят, что обновленная схема помогает покупателю.
2020
25 ноября 2020 года стало известно о том, что российская таможня заблокировала поставки 1,5 млн продуктов Stada из-за сбоя системы маркировки. Подробнее здесь.
Мишустин упростил систему цифровой маркировки лекарств после критики
В начале ноября 2020 года премьер-министр Михаил Мишустин подписал постановление Правительства РФ, которое упрощает систему цифровой маркировки лекарств. Порядок работы стал проще после того, как система подверглась критике из-за постоянных сбоев.
Теперь в аптеках и медицинских учреждениях можно будет выводить лекарства из оборота через кассы сразу после уведомления о поступлении препаратов. Раньше нужно было ждать подтверждения о регистрации лекарств в системе.

Михаил Мишустин упростил систему цифровой маркировки лекарств после шквала критики
До 1 июля 2021 года дополнительно вводятся упрощённые механизмы «обратной приёмки лекарств» при их ввозе в Россию и обороте внутри страны:
Эти сведения будут автоматически подтверждаться самой системой путём проверки кода товара и данных участника. Это повысит скорость операций с препаратами для всех участников, так как снижает зависимость от задержек на стороне поставщиков лекарств.
Упрощенный режим маркировки распространяется на все лекарства, за исключением лекарств из категории 12 высокозатратных нозологий.
Кроме того до 1 февраля 2021 года производители будут наносить коды на препараты, аптеки их должны сканировать, а операции внутри страны станут проще. Все сведения нужно будет заносить в систему, но производить дальнейшие действия с препаратами можно не дожидаясь ответа, если он не получен в течение 15 минут.
В России назревает лекарственный кризис из-за сбоя системы маркировки
В России назревает лекарственный кризис из-за сбоя системы маркировки. Компании не могут поставить более 40 млн упаковок препаратов, среди которых «жизненно необходимые», заявили в Ассоциации международных фармпроизводителей (AIPM).
Как сообщает РБК со ссылкой на опрос AIPM, на сбои пожаловались две трети участников ассоциации — всего там состоят более 60 компаний, которые производят более 80% всех лекарств в мире. Проблемы возникают с поставками в аптеки и в медицинские учреждения.

В РФ назревает лекарственный кризис со сбоем системы маркировки
По словам экспертов Института государственного и муниципального управления НИУ ВШЭ, к концу октября 2020 года поставка 4,5 млн лекарственных препаратов суммарно задержана на 216 дней. По мнению заместителя директора Института государственного и муниципального управления НИУ ВШЭ Константина Головщинского, основными причинами дефицита медикаментов, помимо сбоя в работе системы маркировки, являются проблемы с госзакупками.
27 октября 2020 года Минпромторг перевел систему маркировки на уведомительный режим работы до тех пор, пока участники рынка не будут полностью к ней готовы.
Как признал глава ведомства Денис Мантуров, дистрибуторы лекарств и ряд аптечных организаций оказались технически не готовы к работе с маркированными препаратами, что на фоне повышенного спроса привело к исчезновению лекарств с аптечных полок. Уведомительный порядок существенно смягчил ситуацию.
Бизнес пожаловался Мишустину на систему мониторинга лекарств
В октябре 2020 года Ассоциация международных фармпроизводителей (AIPM), Ассоциация российских фармпроизводителей (АРФП), «Росмедпром», Ассоциация производителей фармацевтической продукции и медицинских изделий (АПФ), Всероссийский союз общественных объединений, Национальная фармацевтическая палата, «Инфарма», «СоюзФарма», Ассоциация независимых аптек и Российская ассоциация аптечных сетей направили премьер-министру Михаилу Мишустину, председателю Совета Федерации Валентине Матвиенко и председателю Госдумы Вячеславу Володину письмо, в котором пожаловались на сбой в работе информационной системы мониторинга движения лекарственных препаратов для медицинского применения (ИС МДЛП).

Бизнес пожаловался Михаилу Мишустину на систему мониторинга лекарств
Бизнес, как пишет Forbes со ссылкой на этот документ, указал на «катастрофическую неработоспособность» системы отслеживания движения лекарств и потребовал оперативных решений, чтобы «предотвратить коллапс системы лекарственного обеспечения», который чреват «самыми негативными последствиями».
Московские фармзаводы внедрили системы обязательной маркировки
Фармацевтические заводы Москвы своевременно завершили тестирование и внедрили системы маркировки лекарственных средств, которая стала обязательной с 1 июля 2020 года. Об этом 6 июля 2020 года сообщил ДИиПП Москвы.
Маркировка необходима для передачи данных о движении лекарственных препаратов – ввод лекарств в оборот, их перемещение от производителя к поставщику и далее в аптеку, временный вывод из обращения и другие операции.
Международная независимая фармацевтическая компания «Сервье» своевременно завершила серию процедур тестирования и валидации систем прослеживаемости движения лекарственных средств, произведенных на заводе в России: с момента запуска системы компания произвела уже более 1 млн промаркированных упаковок, большую часть из которых составляют препараты для лечения сердечно-сосудистых заболеваний и сахарного диабета.
Обязательная цифровая маркировка лекарств вступила в силу в России
1 июля 2020 года вступила в силу обязательная цифровая маркировка лекарств в России. Оборот немаркированных препаратов возможен только для особых случаев после согласования с Росздравнадзором.
Исключения могут быть сделаны только для лекарственных средств за исключением продуктов для медицинского применения, предназначенных для обеспечения лиц, больных гемофилией, муковисцидозом, гипофизарным нанизмом, болезнью Гоше, злокачественными новообразованиями лимфоидной, кроветворной и родственных им тканей, рассеянным склерозом, лиц после трансплантации органов и тканей. Такие препараты должны быть произведены за пределами РФ до 1 октября 2020 года.

Правительство России сможет делать точечные исключения при маркировке лекарств, выпущенных до 1 октября 2020 года
Для определения того, разрешать ли оборот немаркированных лекарств, при Росздравнадзоре создается специальная межведомственная комиссия. Туда войдут представители Минздрава, Минпромторга, Федеральной таможенной службы, ФАС и оператора системы мониторинга.
По словам генерального директора АРФП Виктора Дмитриева, производители опасаются сопутствующего введению маркировки дефицита лекарств в стране.
Вакцины от коронавируса будут подлежать цифровой маркировке
Вакцины от коронавируса COVID-19 в России будут подлежать цифровой маркировке. Об этом в ходе прямой линии по маркировке, организованной Центром развития перспективных технологий (ЦРПТ, оператор системы маркировки товаров), 25 июня 2020 года сообщил заместитель руководителя департамента цифрового развития и информационных технологий Минздрава Евгения Меркулова. Подробнее здесь.
В системе цифровой маркировки лекарств могут ввести мораторий на нарушения
24 июня 2020 года стало известно, что для участников системы цифровой маркировки, которая с 1 июля станет обязательной для лекарств, обуви и табака, может быть введен мораторий на привлечение к ответственности за нарушения. Об этом заявила директор департамента общего бизнес-анализа Центра развития перспективных технологий (ЦРПТ) Вера Волкова во время онлайн-конференции по маркировке, которую организовала Торгово-промышленная палата РФ. Подробнее здесь.
«Сервье» завершила тестирование системы маркировки и прослеживаемости движения лекарств
18 июня 2020 года компания «Сервье» сообщила, что совместно с партнёром в области логистики и информационных систем, компанией «Сантэнс Сервис», завершила валидацию процессов обработки и дистрибьюции сериализованных лекарственных препаратов на платформе 3PL (Third Party Logistics). В ходе PQ-тестирования в продуктивной среде производилась проверка процессов приёмки, внутрискладских операций и отгрузки. В результате компания «Сервье» осуществила поставку партии лекарственных препаратов на склад дистрибьютора «ФК ПУЛЬС».
По информации компании, на каждом этапе, включая приёмку дистрибьютором, данные о лекарственных препаратах передавались в систему МДЛП благодаря используемому ИТ-решению CHECK, TRACK & TRACE (CTT). Подробнее здесь.
Фармкомпания «Норман» внедрила на складе модуль интеграции с ФГИС МДЛП
16 июня 2020 года компания InStock Technologies сообщила, что внедрила на склад фармацевтической компании ООО «Норман» модуль интеграции с МДЛП InStock ФГИС для работы с Обязательной маркировкой лекарств. Подробнее здесь.
Российское подразделение Italfarmaco готово к отправке сообщений в ИС МДЛП
9 июня 2020 года компания Utrace сообщила о завершении внедрения облачного решения для комплексного управления маркировкой товаров L4 Utrace Hub в ООО «ИТФ» (российское подразделение Italfarmaco). Запуск первых партий ожидается в сентябре 2020 года, система полностью готова к их обработке и отправке сообщений в ИС МДЛП. Подробнее здесь.
Разработка мобильного приложения для малого бизнеса
27 мая 2020 года Центр развития перспективных технологий (ЦРПТ) сообщил об инвестировании в разработку мобильного приложения, предназначенного для работы в системе маркировки лекарственных средств. Об этом сообщает ТАСС со ссылкой на пресс-службу компании.
ЦРПТ вложился в создание сервиса, который позволяет работать в системе маркировки лекарств через веб-интерфейс, а также своим мобильным приложением для смартфона заменяет 2D-cканер. Сколько денег было потрачено на этот проект, не уточняется.

Мелкие медорганизации в России будут работать с системой маркировки лекарств через бесплатное мобильное приложение
Решение предназначено в первую очередь для участников рынка, у которых нет оборудования, в том числе 2D-сканеров и товарно-учетных систем, либо товарно-учетные системы не интегрированы с системой мониторинга движения лекарственных препаратов (МДЛП).
По сообщению пресс-службы ЦРПТ, запрос на подобный сервис был получен со стороны медицинских организаций с относительно небольшим объемом оборота лекарств, в том числе стоматологий, небольших медицинских организаций и санаториев.
Перенос сроков обязательной маркировки лекарств
28 мая 2020 года стало известно о переносе сроков введения обязательной маркировки лекарственных средств России из-за пандемии коронавируса COVID-19. Минздрав, Росздравнадзор и Минпромторг направили в Госдуму документ, из которого следует, что ведомства прорабатывают предложение о новой дате запуска проекта.
Как сообщили авторы документа, к концу мая 2020 года из-за сложной эпидемиологической ситуации есть риск, что субъекты обращения препаратов не смогут подготовиться к введению маркировки в установленные сроки, передаёт РИА Новости.

Срок введения обязательной цифровой маркировки лекарств в России передвинут с 1 июля 2020 года на более позднюю дату
Оборот лекарств без цифровых кодов должен быть запрещен в России с 1 июля 2020 года, при этом поступившие в оборот до того времени немаркированные лекарства можно будет продавать до истечения сроков годности.
ЦРПТ (оператор системы маркировки) не ведет обсуждений о переносе срока обязательной маркировки лекарств, заявил заместитель гендиректора ЦРПТ Реваз Юсупов. По его словам, никаких подобных писем или предложений от регуляторов к компании не поступало. Система готова к прослеживаемости всех лекарств с 1 июля, что доказало и недавнее тестирование с нагрузкой в 10 раз выше годового оборота лекарств, заявил Юсупов.
Переносить сроки не имеет смысла: большинство участников оборота готово, к системе подключены 98% российских и 83% иностранных производителей, почти все бюджетные медорганизации, аптеки и дистрибьюторы, продолжает он. В ЦРПТ считают, что очередной перенос станет дискриминацией для большинства участников рынка.
Фарм- и медкомпании в России смогут получать лицензии только после подключения к системе цифровой маркировки
18 мая 2020 года Правительство РФ утвердило постановление, согласно которому фармацевтические и медицинские компании в России смогут получать лицензии только после подключения к системе цифровой маркировки.

С 1 июля маркировка будет лицензионным требованием для производителей лекарств
Документ кабмина РФ, опубликованный на официальном интернет-портале правовой информации, дополняет перечень лицензионных требований, предъявляемых к лицензиату при осуществлении деятельности по производству лекарственных средств, следующим пунктом: «регистрация в системе мониторинга движения лекарственных препаратов для медицинского применения». Постановление вступит в силу 1 июля 2020 года, когда должна заработать обязательная маркировка лекарств (она неоднократно переносилась).
Ранее Ассоциация российских фармпроизводителей обратилась с письмом к председателю Госдумы Вячеславу Володину с просьбой отсрочить запуск введения обязательной маркировки препаратов. Введенные на фоне распространения коронавирусной (COVID-19) инфекции ограничительные меры затрудняют завершение тестирования оборудования и обучение специалистов, считают участники рынка.
Рост числа участников оборота лекарств на 21%
27 марта 2020 года стало известно, что Центр развития перспективных технологий, оператор системы маркировки и прослеживания лекарств (МДЛП) сообщил о значительном росте темпов регистрации фармацевтических и медицинских организаций в системе МДЛП.
С начала 2020 года к системе МДЛП подключились 9 691 участников оборота лекарств, рост составил 21%.
На март 2020 года в системе МДЛП зарегистрировано более 56 000 организаций с лицензией на медицинскую или фармацевтическую деятельность, в том числе более 14 000 аптек, во всех регионах России.
Средний темп регистрации в системе МДЛП – от 200 до 500 организаций в неделю. По мере приближения даты обязательной маркировки лекарств темпы растут. В феврале 2020 года ЦРПТ зафиксировал пятикратный скачок регистраций – до 2000 тысяч организаций в неделю.
Biocad внедрил систему маркировки лекарств и настроил взаимодействие с ФГИС МДЛП
25 марта 2020 года SAP CIS сообщил, что компания Biocad внедрила систему SAP Advanced Track and Trace for Pharmaceuticals (ATTP) SAP Track&Trace для маркировки и отслеживания движения лекарственных средств в соответствии с требованиями российского законодательства. Партнером по внедрению выступила компания 3Keys.
Внедрение системы позволило компании обеспечить ежедневное формирование регулярной отчетности по производству и движению сериализованной продукции, настроить взаимодействие с ФГИС МДЛП / ГИС «Маркировка» для запроса и получения кодов маркировки, реализовать интеграцию с партнерами по отслеживанию сериализованной продукции. Подробнее здесь.
В системе маркировки «Честный знак» зарегистрировано 72% лекарств в России
Данные системы цифровой маркировки и прослеживания товаров «Честный Знак» подтверждают высокую готовность фармацевтической отрасли к введению обязательной маркировки лекарств. Об этом стало известно 10 февраля 2020 года.
По состоянию на 5 февраля 2020 г. в системе маркировки лекарств зарегистрировано 6872 наименований лекарственных препаратов, что составляет 72,4% относительно среднего количества наименований препаратов, которые обращались в РФ в 2018 и 2019 гг., по данным Росздравнадзора.
Согласно открытому онлайн каталогу лекарств Росздравнадзора – ЕСКЛП – всего в России выдано 15824 регистрационных удостоверений на различные наименования лекарственных препаратов. Однако, по данным информационного сервиса Росздравнадзора «Сведения о лекарственных средствах, поступивших в гражданский оборот в РФ» за 2018 и 2019 г., из этого числа в России обращалось (производилось и импортировалось) всего 9482 наименований.
Пилотный проект по мониторингу движения лекарств стартовал 1 февраля 2017 г. Поэтапный переход на маркировку всех лекарств установлен с января по июль 2020 г. С 1 июля 2020 г. производители и импортеры лекарств должны наносить цифровой код на каждую упаковку, а все участники оборота обязаны передавать данные о движении маркированных лекарств на каждом этапе их прохождения по товаропроводящей цепочке в систему маркировки.
ФГИС МДЛП предназначена для организации непрерывного мониторинга движения лекарственных препаратов от производителя до конечного потребителя с использованием индивидуальной и групповой кодированной маркировки (сериализация и агрегация) и идентификации упаковок лекарственных препаратов в целях обеспечения эффективного
К сведениям имеют доступ все зарегистрированные в системе мониторинга движения лекарственных препаратов для медицинского применения ней участники Эксперимента (каждый участник имеет доступ к сведениям по товарам, находящимся в его обороте), а также государственные органы, осуществляющие контроль в сфере обращения
В личном кабинете МДЛП можно зайти в «Место хранения» и посмотреть остатки медикаментов
Списать препарат можно в любой момент, то есть если даже вы его уже полностью использовали, вам необходим только доступ к DataMatrix коду, который был нанесен на вторичную упаковку. Важно помнить, что выбытые из оборота лекарственные препараты вы уже не можете никаким образом продать
Вам необходимо в Личном кабинете « Честного знака » заполнить анкету и направить ее в « Честный знак ». На одну клинику, на одно место осуществления медицинской деятельности выделяется один регистратор выбытия бесплатно. По последним данным он доставляется в течение 2 недель
Списание маркированных лекарств Списать лекарства можно по производственному браку, для изготовления медицинских изделий или отбора клинических образцов. Чтобы сделать это, отправьте в ГИС МДЛП прямое 552-сообщение «Вывод по различным причинам» через сервис Контур
