Журнал “Аптека: бухгалтерский учет и налогообложение” № 6/2019
О системе мониторинга движения лекарственных препаратов для медицинского применения и необходимости подключения к ней участников оборота этих препаратов, а также о принимаемых мерах по созданию данной системы мы неоднократно писали на страницах нашего журнала. Теперь пора переходить от теории к практике. И поможет в этом аптекам и аптечным сетям Инструкция по подключению к ИС МДЛП, опубликованная Росздравнадзором в Письме от 20.05.2019 № 01и-1269/19.
Обязанность участия в системе мониторинга.
Организации и ИП, не подключившиеся к ИС МДЛП, с 1 января 2020 года не смогут осуществлять обращение лекарственных препаратов, имеющих маркировку контрольными (идентификационными) знаками DataMatrix.
Ответственность субъектов обращения лекарственных средств.
За производство или продажу лекарственных препаратов для медицинского применения без нанесения средств идентификации, с нарушением установленного порядка их нанесения, а также за несвоевременное внесение данных в ИС МДЛП для медицинского применения или внесение в нее недостоверных данных организации и ИП несут ответственность в соответствии с действующим законодательством.
Кроме того, согласно ч. 2 ст. 15.12 КоАП РФ продажа товаров и продукции без маркировки и (или) нанесения информации, предусмотренной законодательством РФ, в случае если такая маркировка и (или) нанесение такой информации обязательны, а также хранение, перевозка либо приобретение таких товаров и продукции в целях сбыта, за исключением продукции, указанной в ч. 4 названной статьи, влечет наложение штрафа:
Алгоритм подключения к ИС МДЛП.
Для начала работы с ИС МДЛП аптекам и аптечным сетям необходимо выполнить следующие действия (причем некоторые из них могут выполняться параллельно – для ускорения процесса подключения к системе).
* Шаги 1 и 2 – 5 могут выполняться параллельно.
***Следует учесть, что реализацию и вывод из оборота для медицинского применения в местах ответственного хранения зарегистрировать невозможно.
МДЛП: для кого и зачем?
Закон о маркировке движения лекарственных препаратов (МДЛП) вступает в силу с 01.01.2020. В данной статье мы рассмотрим, в каких программах 1С будет поддерживаться МДЛП и для кого этот сервис предназначен.
Приложение (МДЛП) предусмотрено для учреждений с медицинским направлением деятельности, которые ведут свой учёт в программах 1С, отличных от 1С:Медицина. Больничная аптека. Стоит обратить внимание, что оно не предназначается для ведения количественного и суммового учёта лекарственных средств на складах медицинской организации.
Новое приложение будет актуально для:
В рамках закона предполагается маркировать лекарственные препараты с помощью двухмерного штрих-кода (Data Matrix Code), содержащего данные о производителе, импортёре, дате выпуска и дающего возможность отследить путь от производителя до розничного покупателя. Данные сведения будут отражаться в системе (ИС МДЛП), разработанной ФНС. В конце 2018 года проект по маркировке лекарственных препаратов перешёл от ФНС к основному оператору маркировки – Центру развития перспективных технологий (Честный знак).
Что необходимо делать аптекам и медицинским учреждениям:
С помощью специального мобильного приложения каждый житель страны сможет получить информацию о легальности купленного им препарата и всю информацию по нему.
Рассмотрим на примере несколько форм созданий уведомлений в сервисе МДЛП.
Перед обменом с ИС МДЛП организация должна обсудить с поставщиками лекарственных средств, какая схема акцептования будет использоваться при обмене данными с ИС МДЛП: прямая или обратная.
Прямая схема работает следующим образом: поставщик передаёт сведения об отгруженных лекарственных препаратах для организации (покупателя). А она, в свою очередь, получая данные по отгруженным товарам из ИС МДЛП, подтверждает их или отказывается от приёма.
Обратная схема акцептования реализована так: организация отправляет уведомления о приёмке лекарственных средств в ИС МДЛП. А поставщик, получая данные о принятых товарах, либо подтверждает, либо отказывается от подтверждения этих данных.
В программе при прямом порядке организация получает уведомление от ИС МДЛП, а при обратном – создаёт уведомление сама по кнопке «Создать» на рабочем месте МДЛП (рис. 1, 2, 3).
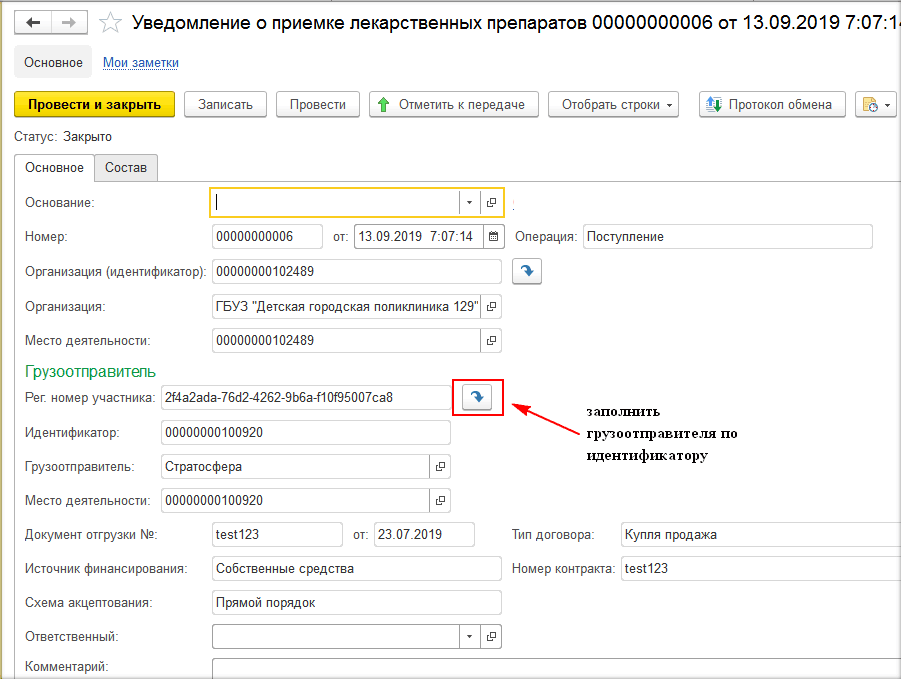
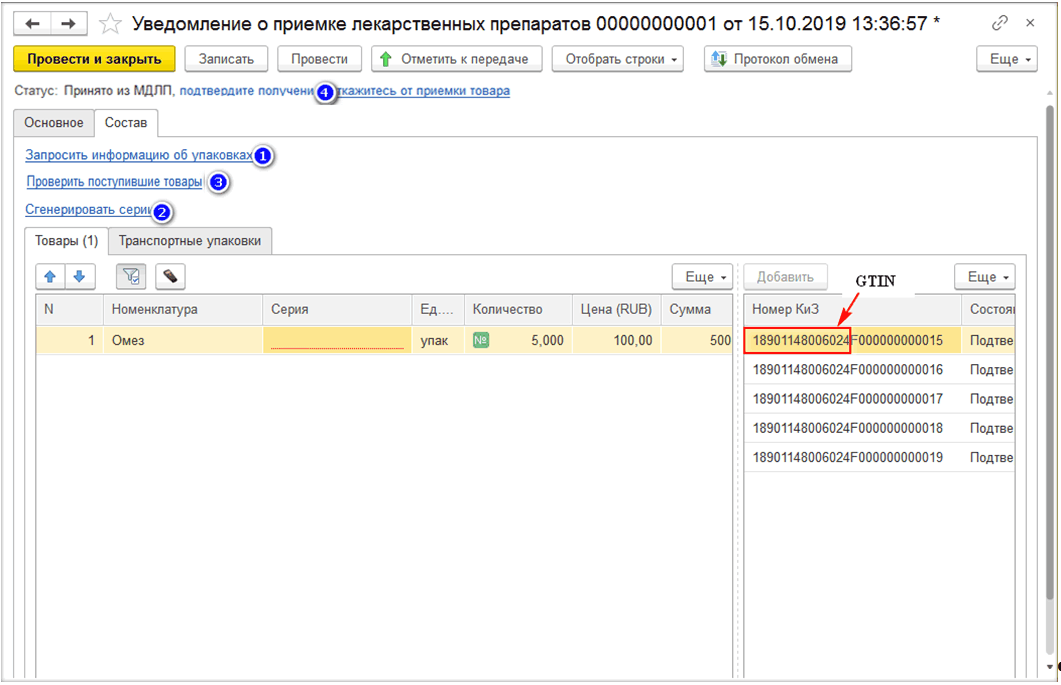
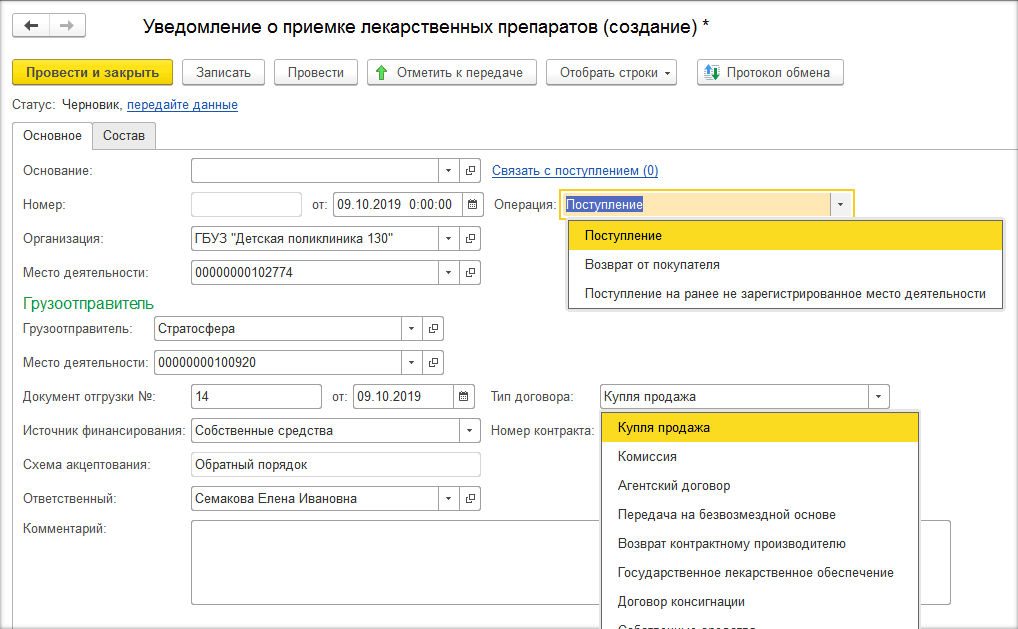
При отгрузке лекарственных средств (при создании уведомления об отгрузке товаров) необходимо на закладке «Основное» заполнить данные отправителя и получателя. Если товар передаётся контрагенту, который не зарегистрирован в системе МДЛП, то необходимо поставить необходимую галочку и выбрать необходимую информацию во вкладках «Операция» и «Тип договора» (рис. 4, 5).
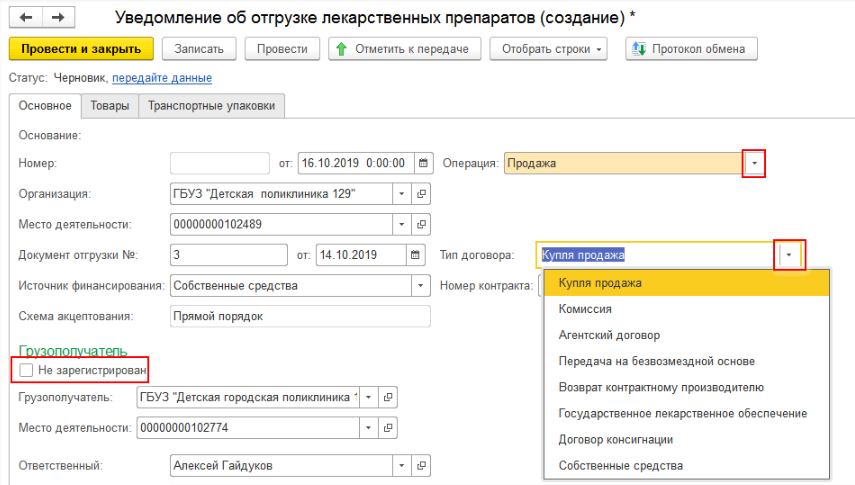
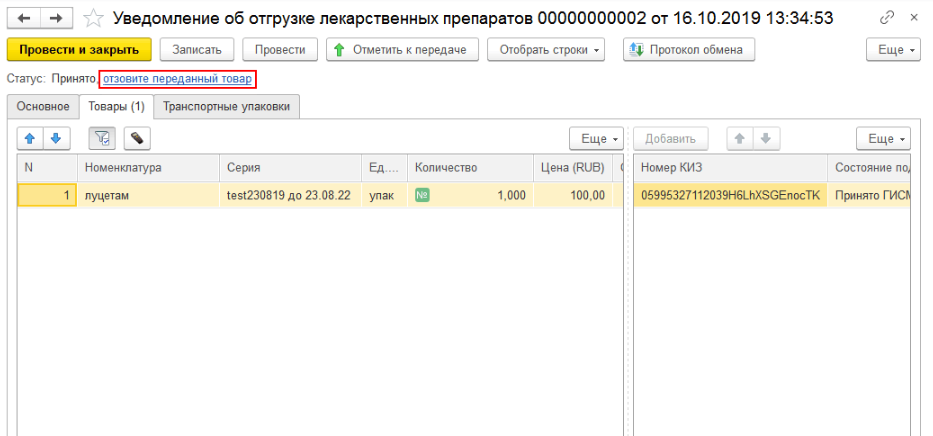
На вкладке «Товары» необходимо просканировать отгружаемые упаковки, либо загрузить номера КиЗ из ТСД, либо ввести вручную по кнопке «Добавить» и передать данные в ИС МДЛП. После произведённого обмена с системой до подтверждения получателем информации об отгрузке можно отозвать переданные товары. Если отгружается транспортная упаковка, то её код вносится на закладке «Транспортные упаковки».
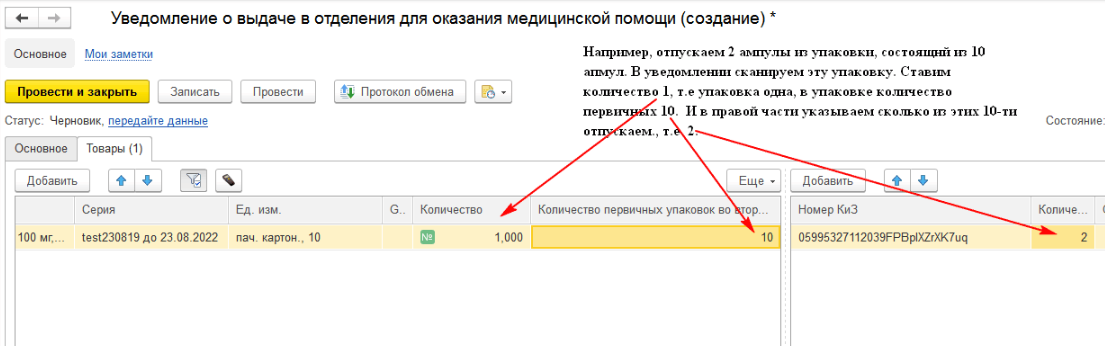
Для того, чтобы лекарственные препараты могли быть перемещены в отделение организации, необходимо создать уведомление о выдаче в отделение для оказания медицинской помощи. На закладке «Основное» заполняем все необходимые сведения. Если в 1С подключён регистратор выбытия, то необходимо поставить галочку «Использовать РВ». Уведомления о выдаче для оказания медицинской помощи будут передаваться в ИС МДЛП через РВ.
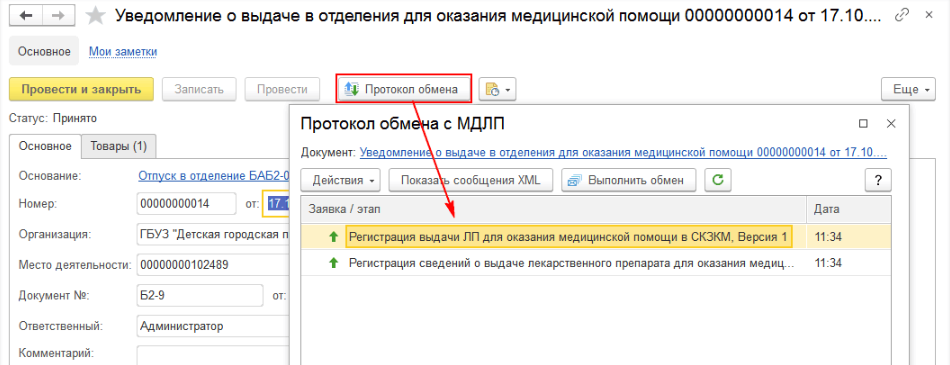
После успешной отправки уведомления можно просмотреть «Протокол уведомлений» (рис. 7).
В данной статье мы ответили на основные вопросы, с которыми может столкнуться пользователь на начальном этапе работы с сервисом МДЛП. Если у вас возникнут сложности с настройкой сервиса, то вы можете обратиться к нашим специалистам, которые выполнят настройки программы 1С с учётом ваших пожеланий. Настройка программ 1С доступна в рамках тарифов сопровождения 1С и как отдельная услуга.
Маркировка лекарственных препаратов (ИС – МДЛП)
Постановление Правительства РФ от 14.12.2018 N 1556 (ред. от 30.06.2021) «Об утверждении Положения о системе мониторинга движения лекарственных препаратов для медицинского применения»
Постановление Правительства РФ от 30.06.2021 N 1069 «О внесении изменений в Положение о системе мониторинга движения лекарственных препаратов для медицинского применения»

ИС “МДЛП” – Информационная система мониторинга движения лекарственных препаратов.
Выделенная линия для аптек и медицинских организаций (Честный знак)
Федеральный закон от 6 апреля 2011 г. N 63-ФЗ “Об электронной подписи”;
Федеральный закон от 28.12.2017 года № 425-ФЗ «О внесении изменений в Федеральный закон «Об обращении лекарственных средств»;
Федеральный закон от 15.04.2019 № 58-ФЗ «О внесении изменений в Кодекс Российской Федерации об административных правонарушениях» (начало действия документа 01.07.2020)
остановления Правительства Российской Федерации:
Постановление Правительства РФ от 15.05. 2020 № 688 «О внесении изменения пункт 5 Положения о лицензировании медицинской деятельности (за исключением указанной деятельности, осуществляемой медицинскими организациями и другими организациями, входящими в частную систему здравоохранения, на территории инновационного центра «Сколково»)»;
Постановление Правительства РФ от 30.06.2020 N 955 «Об особенностях ввода в гражданский оборот лекарственных препаратов для медицинского применения» (срок действия документа ограничен 1 января 2021 года);
Постановление Правительства РФ от 26 ноября 2018 г. № 1416 «О порядке организации обеспечения лекарственными препаратами лиц, больных гемофилией, муковисцидозом, гипофизарным нанизмом, болезнью Гоше, злокачественными новообразованиями лимфоидной, кроветворной и родственных им тканей, рассеянным склерозом, гемолитико-уремическим синдромом, юношеским артритом с системным началом, мукополисахаридозом I, II и VI типов, лиц после трансплантации органов и (или) тканей, а также о признании утратившими силу некоторых актов Правительства Российской Федерации»
Постановление Правительства РФ от 31.12. 2019 № 1954 «О внесении изменений в постановление Правительства РФ от 14.12.2018 № 1556»;
Постановление Правительства РФ от 28.08. 2018 № 1018 «О внесении изменений в постановление Правительства РФ от 24.01.2017 № 62»;
Постановление Правительства РФ от 14.12.2018 № 1556 «Об утверждении положения о системе мониторинга движения лекарственных препаратов для медицинского применения»;
Постановление Правительства РФ от 14.12.2018 № 1557 «Об особенностях внедрения системы мониторинга движения лекарственных препаратов для медицинского применения»;
Постановление Правительства РФ от 14.12.2018 № 1558 «Об утверждении правил размещения общедоступной информации, содержащейся в системе мониторинга движения лекарственных препаратов для медицинского применения, в информационно-телекоммуникационной сети “Интернет” (в том числе в форме открытых данных);
Постановление Правительства РФ от 07.08.2019 № 1027 «О внесении изменения в постановление Правительства РФ от 24.01.2017 № 62;
Распоряжение Правительства РФ от 18.12.2018 № 2828-р «Об определении ООО «Оператор-ЦРПТ» уполномоченным на осуществление функций оператора системы мониторинга движения лекарственных препаратов для медицинского применения»;
Постановление Правительства РФ от 30.08.2019 № 1118 «О внесении изменений в Положение о системе мониторинга движения лекарственных препаратов для медицинского применения» (утвержденное постановлением Правительства РФ от 14.12.2018 № 1556);
Подробно ознакомиться с материалами документации можно на сайте оператора системы маркировки.
Порядок регистрации в ИС МДЛП
Инструкция по формированию заявок на оснащение оборудованием и заполнению заявлений о присоединении к Договорам безвозмездного пользования движимым имуществом
Порядок регистрации в информационной системе мониторинга движения лекарственных препаратов (ИС МДЛП)
Регистрация в информационной системе мониторинга движения лекарственных препаратов (ИС МДЛП)
Для успешной подготовки к регистрации организациям в ИС МДЛП необходимо убедиться в выполнении следующих условий:
Проверить сведения в и можно на сайте ФНС России.
Проверить сведения о лицензиях можно:
Для регистрации в Личном кабинете участника ИС МДЛП, рекомендуется осуществить следующие действия:
Рисунок 1- адресная строка веб-браузера Internet Explorer 11
После перехода по данной ссылке, откроется портал национальной системы цифровой маркировки (см. рисунок 2).
Далее надо перейти в раздел «Маркировка лекарств», с главной страницы портала цифровой маркировки это можно сделать, нажав на пиктограмму лекарств в блоке информации «Подробная информация об обязательной маркировке и экспериментах» – «Маркировка»(см. рисунок 3).
Рисунок 3 – Стрелкой выделена пиктограмма лекарственных препаратов, при нажатии на которую откроется раздел «Маркировка лекарств»
Вы перейдете в раздел «Маркировка лекарств». На данной странице представлена информация от национальной системы цифровой маркировки «Честный знак» в части маркировки лекарственных препаратов (см. рисунок 4).
Рисунок 4 – Раздел «Маркировка лекарств»
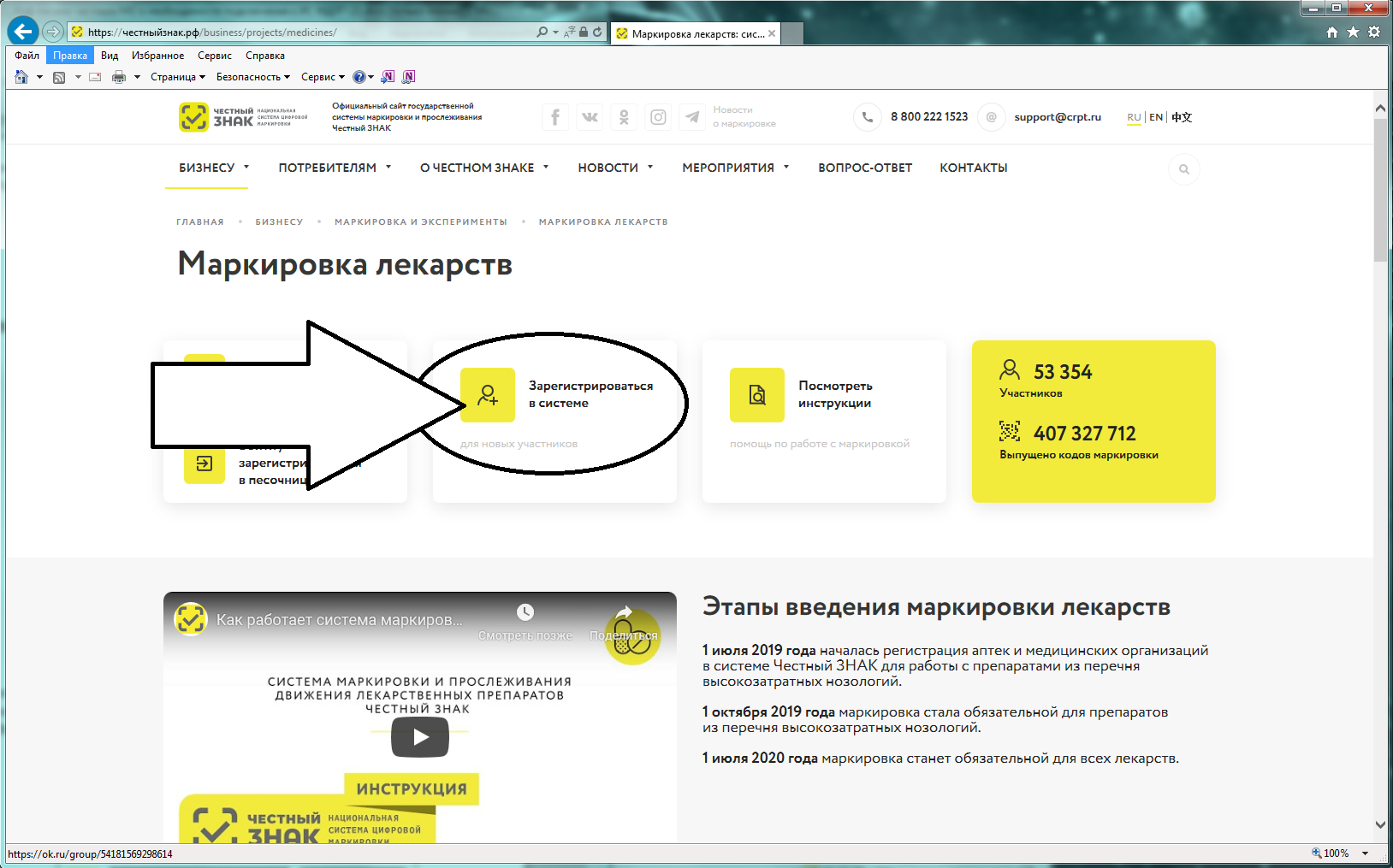
Рисунок 5 – Стрелкой выделена кнопка входа в ИС МДЛП
Если ваше интернет-соединение медленное, скорее всего вы увидите следующее изображение (см. рисунок 6)
Рисунок 6 – скриншот анимации загрузки страницы входа в ИС МДЛП (отображается при медленном подключении к интернету)
На странице входа в систему необходимо нажать на ссылку для регистрации в системе (см. рисунок 7).
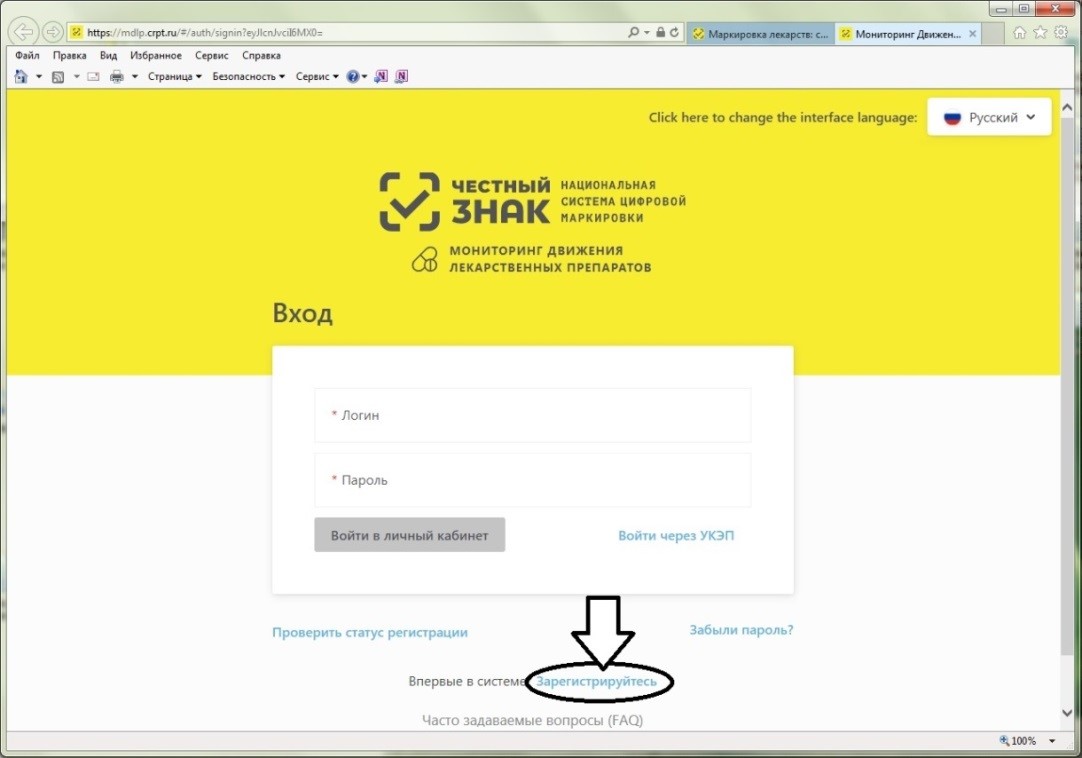
Рисунок 7 – Стрелкой выделена ссылка для регистрации в ИС МДЛП
Откроется страница регистрации в системе (см. рисунок 8).
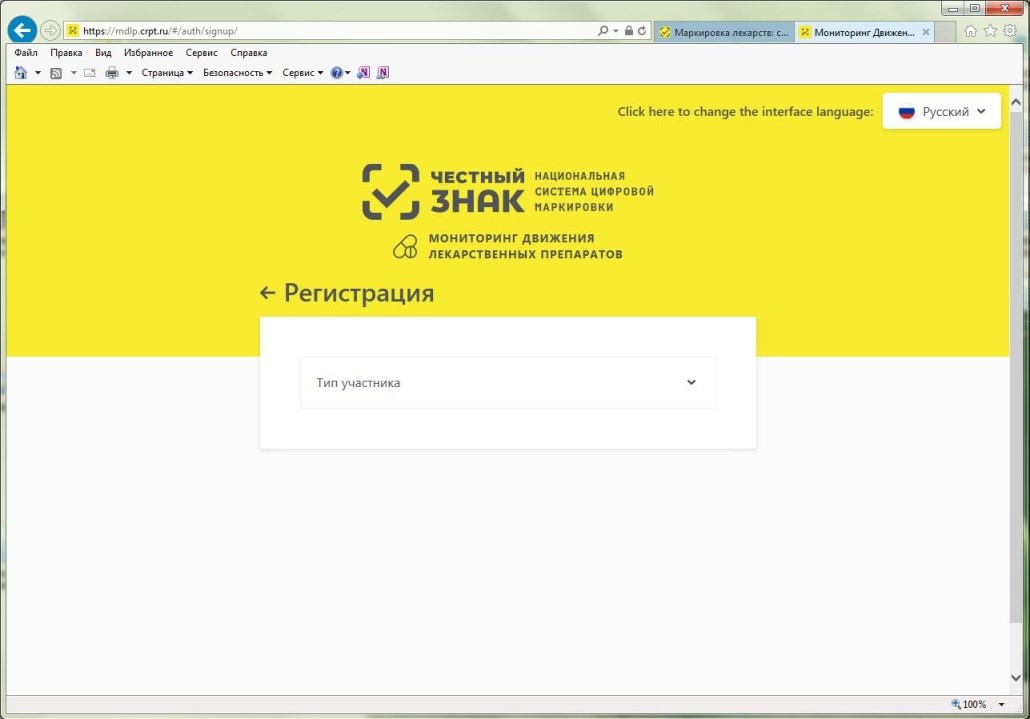
Рисунок 8 – Страница регистрации в ИС МДЛП
После выбора типа участника, система запросит необходимое программное обеспечение (см. рисунок 9).
Далее, при необходимости, следует установить программное обеспечение, сертификаты ключей электронной подписи и выполнить настройки программного обеспечения.

Рисунок 9 – ИС МДЛП запрашивает необходимое программное обеспечение для работы в системе.
Ниже представлены требования программного обеспечения в виде списка:
Далее вам понадобится , откройте пункт 2 раздела 2.2.1 и следуйте дальнейшим инструкциям.

Где получить информацию и задать вопросы о регистрации в cистеме мониторинга движения лекарственных препаратов

Service is not available in your region
Sorry for the inconvenience caused
~ 1 мин на чтениеНет времени читать?
отправить на почту
Что нужно для регистрации в системе ИС МДЛП
1. Наличие усиленной квалифицированной электронной подписи (УКЭП), оформленной на руководителя организации. Если у организации нет УКЭП, то ее можно оформить в одном из удостоверяющих центров, также можно оформить ее через сервис «1С-Подпись».
2. Полное соответствие ФИО руководителя и ИНН организации, указанные в УКЭП, сведениям, внесенным в ЕГРЮЛ/ЕГРИП/РАФП. Проверить сведения в ЕГРЮЛ/ЕГРИП можно на сайте ФНС России. Проверить сведения в РАФП можно на сайте ФНС России.
3. Для регистрации в Личном кабинете участника ИС МДЛП — выполните следующие действия:
Зайдите на портал системы мониторинга движения лекарственных препаратов для медицинского применения.
При необходимости установите программное обеспечение, сертификаты ключей электронной подписи и выполните настройки программного обеспечения.
Нажмите на кнопку «Проверка доступа» — система автоматически проверит возможность подключения компьютера и предоставит инструкции по дальнейшей настройке.
Пример расчета стоимости для автоматизации аптеки с учетом подключения к ИС МДЛП
ЭЦП — от 600 руб/год
«1С: Розница 8. Аптека» — от 26 400 руб.
2D-сканер — от 3 500 руб.
Установка и настройка ПО — от 5 000 руб.
Сопровождение — от 2 818 руб/мес.
Как настроить подключение Фарма. Просто к ФГИС МДЛП?
Обязательным условием регистрации в Системе является уже зарегистрированная организация в ИС МДЛП. Также в ИС МДЛП должен быть добавлен сертификат пользователя, с которым осуществляется регистрация.

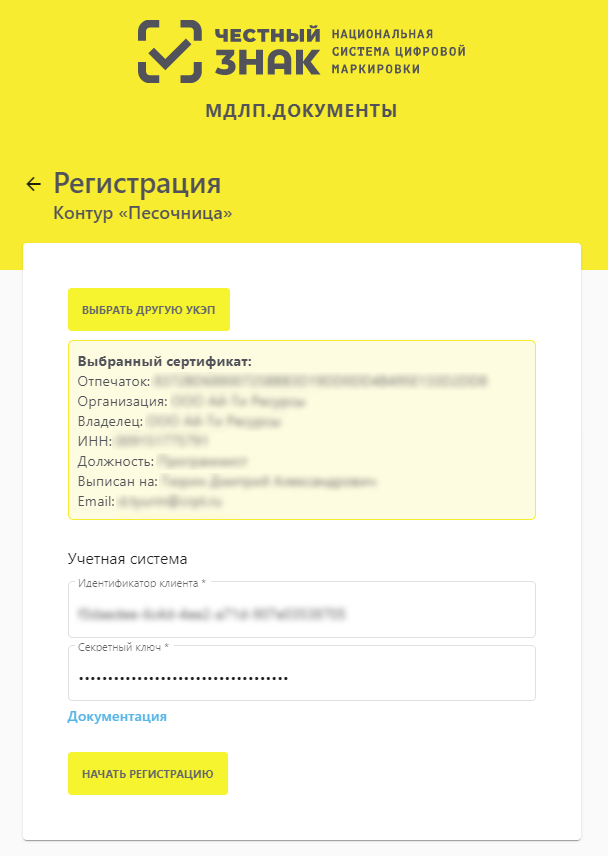
Для регистрации в Системе требуется перейти на страницу регистрации. В открывшемся окне требуется нажать кнопку Регистрация через УКЭП

После нажатия на кнопку появится список доступных сертификатов. Выбираем нужный и нажимаем кнопку Выбрать сертификат.
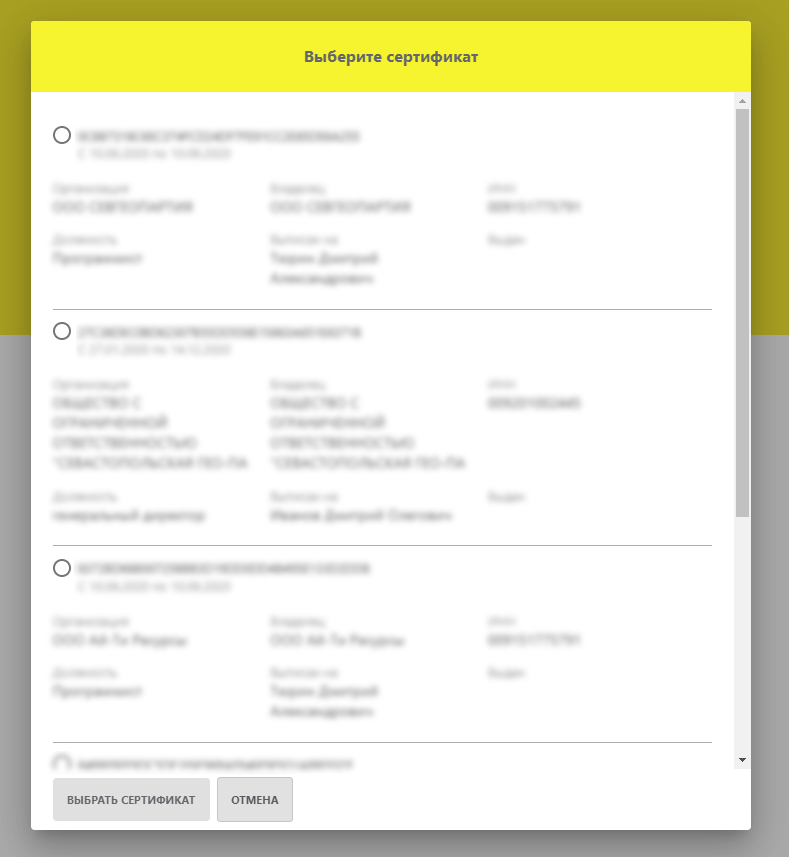
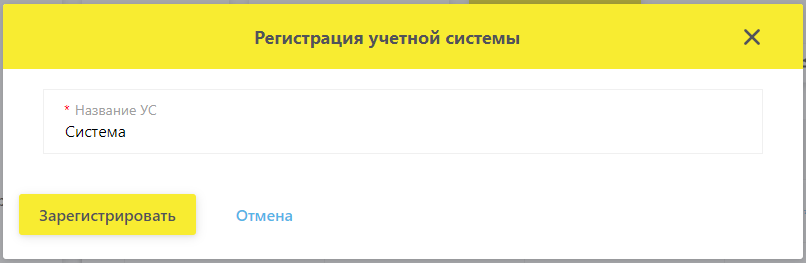
6. После этого будет показано окно “Регистрация завершена”. В этом окне требуется скопировать два значения “Идентификатор клиента” и “Секретный ключ”
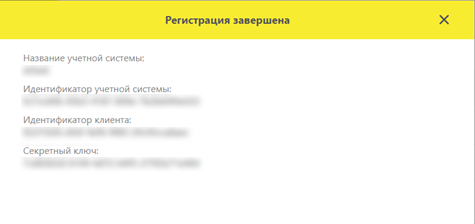
Далее необходимо вернуться на страницу регистрации в Системе, где необходимо заполнить поля “Идентификатор клиента” и “Секретный ключ” и нажать кнопку Начать регистрацию.

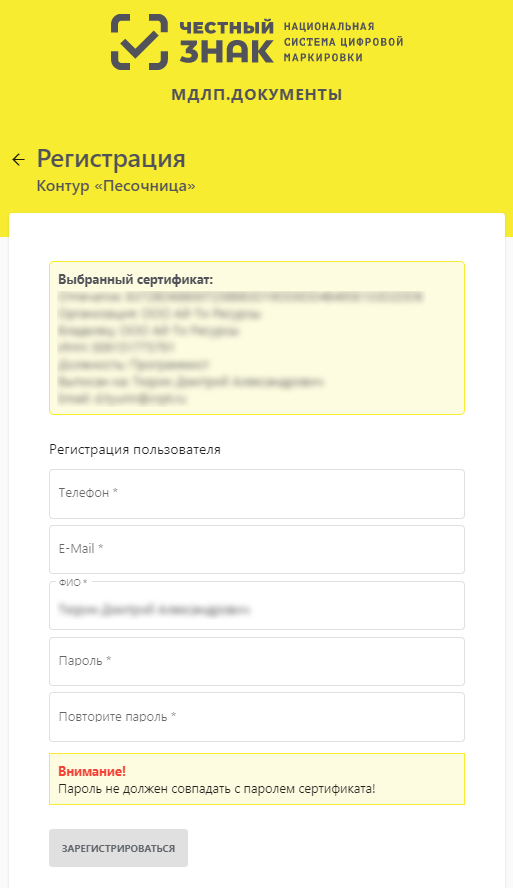
На указанный при регистрации E-Mail будет направлено письмо с данными для доступа в сервис.
После регистрации, можно переходить на страницу Авторизация пользователя.
Ошибка аутентификации
У меня программа 1С бухгалтерия 8.3. (релиз 3.03.37.25). Очень часто, по утрам просто выбрасывает из программы минуты через три после открытия. Пишет «1С будет закрыта. » потом виндовс пытается найти ошибку. «
Посоветуйте, что можно сделать!
вот договоритесь с виндовс чтобы ошибку не выдавалю
Не заметили какую-либо закономерность, во время какого действия это происходит. Или просто, ничего не делаете и программа падает?
Там, наверное, побольше написано. И что в предыдущих записях?
Сейчас релиз 3.03.37.25. Но ошибка не связана с релизом, т.к. выбрасывало из программы и при предыдущем релизе. Самое интересное, что это началось как-то утром. И у нас 3 компьютера в сети с 1С бух., вот на одном компьютере 1С не выбрасывает, а в двух других постоянно. вот сегодня например, выкинуло раза 4, а потом все работало. Смотрели сеть, там все ОК.
пользователи с одними и теми же правами? в одной и той же программе? утром никакого резервирования баз нет? может что то по расписанию задано..
lew1, нажми на кружочек с вопросом и посмотри платформу
На картинке сложно что-либо разглядеть. Можете выложить картинку в родном разрешении экрана (без сжатия)? 3. Каким образом выполняется авторизация пользователей: вы указываете имя пользователя (и, возможно, пароль) при входе в 1С, или используются имена пользователей Windows, или никакой авторизации пользователей нет.
нет такой платформы..на кнопочку нажмите- показать информацию о программе и там посмотрите
Действуем по инструкции
Я купила отдельно у компании 1С «Учет ГСМ» и поэтому релиз я скачиваю с их сайта, т.е. после того как 1С выпускает свой релиз, эта фирма 1С франчайзи «вставляет» сою доработку в основной релиз и я его скачиваю. Но доработку эту я купила в октябре этого года, а глючить начало недели две назад.
Нештатные ситуации в системе МДЛП
Компания «ЦРПТ» поясняет сложные моменты работы с системой маркировки в аптеках и ЛПУ
30 сентября на нашем сайте состоялся вебинар от оператора системы мониторинга движения лекарственных препаратов компании «ЦРПТ», на котором эксперт компании рассказал об общих подходах к решению нештатных ситуаций, возникающих при работе с ГИС МДЛП. К сожалению, из‑за ограниченного времени вебинара и большого количества участников, лектор не успел ответить на все заданные вопросы. Для тех, кто по каким‑либо причинам пропустил трансляцию, мы приводим ее краткий обзор и ответы на вопросы, заданные во время эфира.
Общие решения для нештатных ситуаций при работе с системой маркировки
По данным компании ЦРПТ, больше всего проблем у пользователей возникает в процессе выбытия лекарственных препаратов из оборота. Самый частый вопрос: «Если система недоступна, проводятся технические работ и т. д. — как быть?». Здесь стоит отметить основные моменты, что отпуск возможен двумя способами — продажа через ККТ (т. е. с оформлением чеков) и по регистраторам выбытия. Оба этих способа умеют «накапливать» в себе данные о выбытии и передавать их в систему при появлении соединения с ней.
В первом случае за передачу данных в систему отвечает оператор фискальных данных. Таким образом, при наличии каких‑либо задержек, вызванных теми или иными причинами, аптеки могут не переживать за ответственность, потому что агрегированная информация передается именно оператором.
При использовании регистратора выбытия, даже если ГИС МДЛП недоступна, можно просканировать препараты, и сформировать с помощью регистратора документы о выбытии лекарств из оборота. Они будут отправлены в «буфер», который будет передан в систему МДЛП, когда она станет доступна.
Кроме этого в системе ГИС МДЛП предусмотрен механизм «реестра ожидания», он работает в том случае, когда аптека собирается отпустить лекарственный препарат, однако информация о его приемке не поступила в систему из‑за регламентных работ. В этом случае ЛП можно отпускать, фискальный оператор передаст в систему данные о выбытии, а система, в свою очередь «увидит», что на этот ЛП нет информации, подтверждающей поставку на место деятельности, где был осуществлен отпуск. Тогда, для завершения цикла, информация о выбытии будет находиться в реестре ожидания до получения данных о приемке.
Таким образом, с помощью этого механизма можно отпускать лекарственные средства даже если на момент их приемки система МДЛП была недоступна. Максимальный период ожидания составляет две недели. В этот срок любые технические работы в системе МДЛП будут закончены. Обратите внимание, что механизм «реестра ожидания» работает только при обратном акцепте приемки ЛС.
Также в решении большинства проблемы могут помочь документы, доступные на сайте «Честный знак». В большинстве из них приведены примеры нештатных случаев, а также даны алгоритмы по правильной работе с системой, которые помогут самостоятельно найти и устранить причину возникших трудностей:
Кроме этого, на сайте есть раздел «Обучающий центр», где даны краткие, но подробные видео-инструкции по основным направлениям работы с системой ГИС МДЛП.
Ответы на вопросы
После теоретического вступления перейдем к практическим вопросам участников вебинара:
Как оформить возврат промаркированного товара, если выявлены недостатки после продажи?
Есть такая операция «Возврат в оборот» — ее описание можно найти в «Паспортах процесса». Стоит отметить, что возврат в оборот лекарственного препарата возможен только для последующего возврата поставщику, поскольку он (препарат) будет признан недоброкачественным.
Почему медицинским организациям запретили повторный ввод ЛС в оборот? Планируется ли возобновление данной операции?
Здесь нужно уточнить — повторный ввод после каких операций, и при каких условиях. Например, при выбытии ЛС в рамках стационара он должен быть доступен.
Как в реестре отправленных документов быстро найти необходимый документ?
В реестре есть функция фильтрации, где можно указать критерии поиска по идентификатору организации, ИНН, времени совершения операции и так далее.
Первый раз получили маркированный товар. Пришла товарная единица, содержащая 180 упаковок товара. Не считали код с коробки, а только с каждой упаковки. Коробку после этого выкинули. Теперь выпадает ошибка. Как ее исправить?
Почему данные от поставщиков не приходят в МДЛП? Скопилось много накладных!
Попробуйте с данным вопросом обратиться к поставщику вашей товарно-учетной системы, возможно проблема кроется именно в ней. Также всегда проверяйте по какому акцепту вам поставляется товар — при обратном акцепте вам не должны приходить документы первыми.
Что делать если препарат продан (выбит чек ОФД), а в ГИС МДЛП не прошло выбытие?
Во-первых, нужно убедиться, что этот препарат не значится в реестре ожидания — т. е. нужно проверить, что вы осуществили и подтвердили его приемку. Во-вторых, как уже было сказано ранее, за передачу данных в систему через ККТ отвечает ОФД, а значит это может происходить не мгновенно. И в‑третьих, если проблема сохраняется, об этом можно написать в службу поддержки, указав все необходимые сведения.
Почему нет уведомлений о сбое сервиса и времени проводимых технических работ?
Уведомления о плановых работах ГИС МДЛП приходят на электронный адрес, который организация указала при регистрации. Кроме этого анонсы дублируются в социальных сетях и Telegram-канале.
Из-за ошибки учетной программы два препарата ушли с ошибкой — система их не восприняла. Теперь по учетной они ушли, а по системе остались в обороте, что делать?
Нужно обратиться к вендору учетной системы с вопросом — по какой причине произошла ошибка обработки данных и информация в систему не была передана, а после, совместно с ним, составить обращение в службу технической поддержки ГИС МДЛП. Обращение к поставщику товарно-учетной системы необходимо для заполнения технического описания проблемы, чтобы наши специалисты смогли ее решить.
В МДЛП был отправлен документ об успешном агрегировании. Через какое время агрегированные короба будут отображены в личном кабинете?
Если вы получили квитанцию об агрегировании, то это значит, что система уже обработала данный документ — и, если вы не проводили разеграгации, SGTIN и SSCC будут доступны в кабинете. Если этого не произошло — нужно написать в службу поддержки.
Как изменить идентификатор места деятельности поставщика?
Его нельзя изменить. Он выдается исходя из адреса, указанного в лицензии, выданной Росздравнадзором. Таким образом, при смене адреса места осуществления деятельности, код идентификатора может изменить только сам контрагент.
Если после приемки возникла ошибка обработки пакета, а препарат продан — что тогда?
Если он продан, то SGTIN будут в документах о выбытии. И при возникновении такой ситуации можно написать в службу поддержки и решить эту проблему, имея на руках фактуры приемки, где указан SGTIN этого препарата.
Как вывести препарат из оборота не через кассу и не через регистратора выбытия?
Никак. Это невозможно.
Многие организации по ошибке зарегистрировали лишние места деятельности. Теперь поставщики путаются. Как «почистить» свой список неактивных мест деятельности?
Для начала следует узнать, как вам удалось зарегистрировать ошибочные места деятельности. Для решения этого вопроса следует написать в службу поддержку, чтобы скорректировать список мест деятельности.
Если товар появился на остатке аптеки в «Честном знаке», значит ли это, что приходные операции проведены правильно?
С какого момента начинает свой отчет один рабочий день?
С момента приемки товара, зафиксированного в накладной.
Аптека получила от поставщика препарат с признаками маркировки, передала в систему информацию об этом. В ответ пришла ошибка «Попытка изменить состояние вложенного КИЗ». Поставщик предложил сделать возврат. Аптека может сделать возврат товара как немаркированного?
Такая ошибка возвращается, когда полученные аптекой SGTIN находятся в каком‑либо коробе — т. е. поставщик не разагрегировал транспортную упаковку. В первую очередь нужно просить поставщика найти их у себя на балансе, а потом сделать частичный или полный вывод из SSCC. После этого ошибка исчезнет и операция будет успешно завершена.
При приемке товара выяснилось, что товар в системе значится как «выпущенный в рамках пилотного проекта» — текущего владельца система не выдает. Как аптеке понять, что товаропроводящая цепочка соблюдена?
Если ЛС произведен до 1 июля (кроме препаратов ВЗН), то информация о нем может не передаваться в систему. Чтобы уточнить информацию по поводу соблюдения товаропроводящей цепи, нужно узнать у поставщика по какому акцепту он передавал вам ЛС. И отправить в систему МДЛП данные об успешной приемке. Если на этом ЛС будет ошибка «недопустимая операция для данного SGTIN», то не нужно пугаться — это нормально для ЛС, выпущенных в рамках проекта.
Аптека получает товар по обратному акцепту, сканирует каждую упаковку, поставщики не подтверждают по несколько дней или приходит «Ошибка состояния вложенного КИЗ», которую также не могут исправить по несколько дней. Какие сроки отводятся для устранения ошибок и подтверждения поставщику или производителю? Какие санкции их ждут за нарушения?
Это статья 6.34. Кодекса об Административных правонарушениях.
Аптечная сеть снабжает ФАП по договорам комиссии. Как отгружать ЛС с учетом соблюдения таких документов?
Отгрузку нужно осуществлять по обратному или прямому акцепту, а в типе документа указать «Договор комиссии». Если ФАП не имеет ККТ или регистраторов выбытия, то информацию в ГИС МДЛП должна передавать головная организация.
Аптека получила 4 упаковки с признаком маркировки. Передала данные в систему. На три упаковки пришло подтверждение, а на четвертую — ошибка. Поставщик говорит, что ошибка на стороне производителя. Что делать?
Этого не может быть. Потому что поставщик не мог принять препарат от производителя и не передать сведения об этом в ГИС МДЛП. Нужно решать такие вопросы с поставщиком. Для дополнительной помощи можно обратиться в службу поддержки.
Если проблема с ОФД и данные не переходят в ГИС МДЛП, но препараты уже проданы — является ли это нарушением?
Зависит от типа проблемы. Если не меняется статус в течение первых 10–20 минут, то это нормально, он поменяется позднее.
За сколько дней по закону поставщик должен подтвердить приемку товара?
За один рабочий день.
Программа не дает продать товар — от нас документы ушли в систему, но там не отобразились!
В первую очередь обратитесь к поставщику вашего программного обеспечения, а после, с их помощью, сформируйте запрос с указанием идентификаторов отправленных документов для нашей службы поддержки.
Проблема при акцептовании — поставщик не видит запросов аптеки и приходится перевыкладывать документы, хотя по МДЛП все уходит вовремя!
Опишите подробно эту ситуацию службе поддержки — какие документы уходят, какие поставщик требует вновь. Там проверят, приходят ли уведомления об этом, и решат этот вопрос.
Уронили флакон, разбили одну ампулу — как вывести из оборота данный товар?
Это 552 схема в паспорте процессов — «Списание ЛС или передача на уничтожение».
Если выявлен заводской брак, то как быть?
Есть такая схема в паспорте процессов «Возврат поставщику по причине брака». Можно воспользоваться ей.
Как принимать ЛП, если они пришли в транспортной упаковке и россыпью?
По частям — сначала упаковка, потом добавляете то, что пришло россыпью. Поставку можно оформлять несколькими документами.
При обращении в службу поддержки попросили предоставить открытый ключ в формате CER. Что это?
Для этого надо зайти в программу «КриптоПро», найти «Хранилище сертификатов» и сделать его экспорт. Подробное описание этого процесса есть в разделе «Обучающий центр» на сайте ЦРПТ.
Можно ли сделать автоматическую разагрегацию групповой упаковки, если кассир пытается сделать выбытие первичной упаковки?
Если вы уже приняли эти ЛС на баланс по SSCC и далее не делали разагрегацию группового кода, то вы можете так настроить свою товарно-учетную систему. Запрета на это нет.
Читайте больше полезного по маркировке лекарственных препаратов в специальной рубрике на нашем сайте.
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.
Почему возникает «Ошибка при подписании данных» при отправке отчетности с помощью сервиса «1С-Отчетность»?
При попытке отправить регламентированный отчёт с помощью сервиса «1С-Отчетность» в окне служебных сообщений выдается сообщение «Ошибка при подписании данных». Как исправляется данная ошибка и что предпринять, чтобы она в дальнейшем не возникала?
Ошибка возникает из-за того, что СКЗИ «VipNet CSP» не было зарегистрировано при первоначальном подключении к сервису «1С-Отчетность». Предлагаем ознакомиться с инструкцией по регистрации.
Инструкция по регистрации продукта VipNet CSP.
2. Перед Вами откроется окно следующего вида (рис. 2.), выберите пункт «Зарегистрировать ViPNet CSP» и нажмите кнопку «Далее».
3. В следующем окне выберите пункт «Запрос на регистрацию (получить код регистрации)» и нажмите кнопку «Далее» (рис. 3.).
4. В окне «Способ запроса на регистрацию» (рис. 4.) выберите пункт «Через Интернет (online)». При этом Ваш компьютер должен быть подключен к Интернету. Нажмите кнопку «Далее».
6. Если регистрация прошла успешно, программа установки сообщит об этом (рис. 6.). Нажмите кнопку «Готово».
7. Откроется окно «Настройка ViPNet CSP» (рис. 7.). Нажмите в нем кнопку «ОК».
Почему Честный ЗНАК не видит электронную подпись и другие ошибки ЭЦП
Для работы с маркировкой Честный ЗНАК необходима УКЭП, обычная ЭЦП не подойдет, почему — читайте в статье “Какая подпись нужна для маркировки Честный ЗНАК”. А в рамках этого материала разберемся, почему Честный ЗНАК не видит электронную подпись (УКЭП) и какие еще ошибки могут возникать при использовании электронной подписи (ЭП) в Национальной системе цифровой маркировки и прослеживаемости товаров.
Почему система маркировки Честный ЗНАК не видит УКЭП
«Честный Знак» может не находить электронную подпись при регистрации и авторизации в личном кабинете участника оборота. В этом случае в окне входа появится сообщение: «Внимание! Усиленная квалифицированная подпись (УКЭП) не найдена или не настроено программное обеспечение для работы в системе».
Возникать такая ошибка может по нескольким причинам.
Не вставлена флешка с ЭЦП
Файлы электронной подписи хранятся на внешнем устройстве, если оно не подключено — подпись не работает. Проверьте, вставлен ли носитель с электронной подписью в USB-порт компьютера и насколько надежно соединение.
Не установлено СКЗИ
СКЗИ — это специальная программа, которая формирует электронную подпись и отвечает за безопасное шифрование данных. Расшифровывается аббревиатура как средство криптографической защиты информации. Без этой программы работать с подписью не получится. Выберите и установите криптопровайдер с поддержкой алгоритмов шифрования ГОСТ 34.10-2001, ГОСТ 28147-89, ГОСТ Р 34.11-2012, например, КриптоПро CSP или VipNet CSP.
Не установлен драйвер носителя
Плагин подходит для любых браузеров, если они используют скриптовый язык JavaScript. Вот полный перечень:
Не установлены сертификаты
С помощью сертификата подтверждается подлинность электронной подписи и ее владелец. Установите на устройстве, с которого заходите в «Честный Знак», личный и корневые сертификаты.
Установка личного сертификата
Выбрав нужный файл личного сертификата, нажмите «ОК». Если указать галочку «Найти контейнер автоматически», КриптоПРО сама сопоставит нужный контейнер и сертификат. Остается подтвердить действие после установки сертификата, нажав «Готово».
Установка корневого сертификата
Откройте сохраненный файл и нажмите «Установить сертификат». Дальше следуйте указаниям мастера установки сертификата. Важно правильно задать область хранения файла — хранилище «Промежуточные центры сертификации», чтобы корректно выстроилась цепочка доверия.
Не подтверждена подлинность сертификата
Для проверки подлинности загрузите файл открытого ключа в формате ИМЯ.cer на страницу проверки на сайте ГосУслуг. Если в результате проверки обнаружится, что подлинность не подтверждена, обратитесь в выдавший его УЦ.
Для Linux просмотр списка контейнеров вызывается сервисной программой «csptest». Она находится в директории «/opt/cprocsp/bin/ ».
ФГИС МДЛП предназначена для организации непрерывного мониторинга движения лекарственных препаратов от производителя до конечного потребителя с использованием индивидуальной и групповой кодированной маркировки (сериализация и агрегация) и идентификации упаковок лекарственных препаратов в целях обеспечения эффективного
К сведениям имеют доступ все зарегистрированные в системе мониторинга движения лекарственных препаратов для медицинского применения ней участники Эксперимента (каждый участник имеет доступ к сведениям по товарам, находящимся в его обороте), а также государственные органы, осуществляющие контроль в сфере обращения
В личном кабинете МДЛП можно зайти в «Место хранения» и посмотреть остатки медикаментов
Авторизуйтесь на сайте « Честный знак ». Вставьте в компьютер электронную подпись сотрудника, которому будете предоставлять доступ. Нажмите , перейдите на вкладку « Пользователи » и кликните «+ Добавить пользователя ». Укажите ФИО и email сотрудника
Маркировка лекарств — это нанесение двумерного уникального кода Data Matrix на каждую упаковку. Благодаря ему идентифицируют препарат и отслеживают его перемещение, начиная с момента изготовления и до выбытия из оборота. Реализовать лекарства, если на них отсутствует маркировка , невозможно
Регистратор выбытия – это техническое средство для сканирования DataMatrix-кодов, с помощью которого фиксируется передача лекарственных средств для оказания помощи пациенту. Посредством регистратора данные о выбытии лекарственных препаратов передаются из мед учреждения или аптеки в ГИС МДЛП
Какие документы регламентируют внедрение маркировки лекарств ? С 1 февраля 2017 года на территории Российской Федерации начался эксперимент по маркировке лекарственных препаратов в соответствии с постановлением Правительства Российской Федерации от 24 января 2017 г
